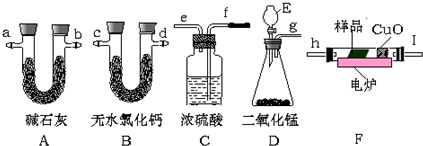
4.下列化学用语或模型不正确的是( )
| A. | 甲烷分子的比例模型: | B. | 氯化氢的电子式:H:Cl | ||
| C. | 乙烷的分子式:C2H6 | D. | 乙烯的结构简式:CH2=CH2 |
3.在C(s)+CO2(g)?2CO(g)的反应中,现采取下列措施:①缩小体积,增大压强 ②增加碳的量 ③通入CO2④恒容下充入He ⑤恒压下充入He ⑥加热其中能够使反应速率增大的措施是( )
| A. | ①④ | B. | ②③⑤ | C. | ①③⑥ | D. | ①②④ |
2.25℃时,水中存在平衡:H2O?H++OH-△H>0,下列叙述正确的是( )
| A. | 加入稀氨水,平衡逆向移动,c(OH-)降低,Kw不变 | |
| B. | 加入少量固体CuSO4,c (H+)增大,Kw不变 | |
| C. | 加入少量固体CH3COONa,平衡逆向移动,c (H+)降低,Kw不变 | |
| D. | 加热到90℃,Kw增大,溶液仍呈中性,pH不变 |
20.为验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验).
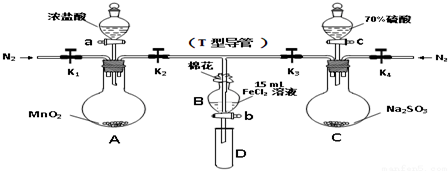
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,加热A.
Ⅲ.当B中溶液变黄时,停止加热,夹紧K2.
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子.
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后夹紧K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子..
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰.
(2)若向第Ⅲ步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式2Fe3++H2S═2Fe2++2H++S↓
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是甲(填“甲”“乙”“丙”)
(5)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入1.12LCl2(标准状况下),若溶液中有$\frac{1}{2}$的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为0.5mol/L.

实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,加热A.
Ⅲ.当B中溶液变黄时,停止加热,夹紧K2.
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子.
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后夹紧K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子..
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰.
(2)若向第Ⅲ步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式2Fe3++H2S═2Fe2++2H++S↓
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是甲(填“甲”“乙”“丙”)
| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
19.下列操作不能说明仪器组装气密性良好的是( )
| A. | 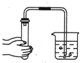 | B. | 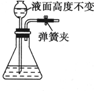 | C. | 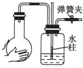 | D. |  |
18.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 100mL 0.1mol•L-1Na2SO4溶液中,钠离子总数是0.2NA | |
| B. | 常温常压下,32gO2中所含电子的数目为16NA | |
| C. | 1mol Al3+含有电子的数目是3NA | |
| D. | 标准状况下,分子数为NA的N2、C2H4混合气体的质量无法确定 |
17.重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放.
I.某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,
且酸性较强.为回收利用,通常采用如下流程处理:

注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见表.
(1)氧化过程中可代替H2O2的最佳试剂是A (填序号).
A.Na2O2 B.FeCl3 C.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是AB(填序号);
已知钠离子交换树脂的原理:Mn++nNaR-→MRn+nNa+,此步操作被交换除去的杂质离子是CD (填序号).
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
II.酸性条件下,六价铬主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水:该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(3)电解时能否用Cu电极来代替Fe电极?不能 (填“能”或“不能”),理由是:因阳极产生的Cu2+不能使Cr2O72-还原到低价态
(4)电解时阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式为:6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O
(5)常温下,Cr(OH)3的溶度积Ksp=1×10-32,当溶液中的c(Cr3+)=10-5 mol•L-1时,pH=5.
I.某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,
且酸性较强.为回收利用,通常采用如下流程处理:

注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见表.
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
A.Na2O2 B.FeCl3 C.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是AB(填序号);
已知钠离子交换树脂的原理:Mn++nNaR-→MRn+nNa+,此步操作被交换除去的杂质离子是CD (填序号).
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
II.酸性条件下,六价铬主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水:该法用Fe作电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(3)电解时能否用Cu电极来代替Fe电极?不能 (填“能”或“不能”),理由是:因阳极产生的Cu2+不能使Cr2O72-还原到低价态
(4)电解时阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式为:6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O
(5)常温下,Cr(OH)3的溶度积Ksp=1×10-32,当溶液中的c(Cr3+)=10-5 mol•L-1时,pH=5.
16.工业废气的氮氧化物(如NO、NO2等,用通式NOx表示)是主要的大气污染物之一.为了保护环境,工业上常通入氨气与之发生如下反应:NOx+NH3→N2+H2O.有关此反应,下列说法中错误的是( )
| A. | N2既是氧化产物又是还原产物 | |
| B. | 反应通式配平为6NOx+4xNH3=(3+2x)N2+6xH2O | |
| C. | 当x=1时,每生成2.5mol N2,被氧化的气体有3mol | |
| D. | 当x=2时,有1mol气体被还原时,转移的电子为4mol |
15.下列实验中,所采取的分离方法与对应原理都正确的是( )
0 158859 158867 158873 158877 158883 158885 158889 158895 158897 158903 158909 158913 158915 158919 158925 158927 158933 158937 158939 158943 158945 158949 158951 158953 158954 158955 158957 158958 158959 158961 158963 158967 158969 158973 158975 158979 158985 158987 158993 158997 158999 159003 159009 159015 159017 159023 159027 159029 159035 159039 159045 159053 203614
| 选项 | 目的 | 分离方法 | 原理 |
| A | 使用CCl4提取碘水中的碘 | 萃取、分液 | 碘在CCl4中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去淀粉胶体中的NaCl | 过滤 | 淀粉胶体不能透过滤纸 |
| D | 分离氯化钠和氯化铵 | 升华 | 氯化铵易升华 |
| A. | A | B. | B | C. | C | D. | D |