3.如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定).
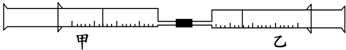
试回答下列问题:
(1)实验1中,沉淀最终变为红褐色色,写出生成白色沉淀的离子方程式:Fe2++2NH3.H2O=Fe(OH)2↓+2NH4+.
(2)实验2中,甲中最后剩余的无色气体是NO,写出NO2与H2O反应的化学方程式3NO2+H2O═2HNO3+NO.
(3)实验3中,已知:3Cl2+2NH3═N2+6HCl.甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为黄绿色变为无色,最后针筒内剩余气体的体积约为5mL.

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒 的现象 |
| 1 | 10mL FeSO4溶液 | 10mL NH3 | 生成白色沉淀,后变色 |
| 2 | 30mL NO2 | 10mL H2O(l) | 剩无色气体 |
| 3 | 15mL Cl2 | 40mL NH3 |
(1)实验1中,沉淀最终变为红褐色色,写出生成白色沉淀的离子方程式:Fe2++2NH3.H2O=Fe(OH)2↓+2NH4+.
(2)实验2中,甲中最后剩余的无色气体是NO,写出NO2与H2O反应的化学方程式3NO2+H2O═2HNO3+NO.
(3)实验3中,已知:3Cl2+2NH3═N2+6HCl.甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为黄绿色变为无色,最后针筒内剩余气体的体积约为5mL.
20.下列说法正确的是( )
| A. | 硫酸工业中涉及的3步反应都为氧化还原反应 | |
| B. | 由反应:H2S+Cl2═S↓+2HCl可知,还原性:Cl2>S | |
| C. | 如用NaOH溶液来吸收尾气中的SO2,只能生成一种盐 | |
| D. | 常温下,铝质容器或铁质容器可储运浓硫酸和浓硝酸 |
19.有科学家提出,硅是“21世纪的能源”,下面有关硅的叙述中,正确的是( )
0 158849 158857 158863 158867 158873 158875 158879 158885 158887 158893 158899 158903 158905 158909 158915 158917 158923 158927 158929 158933 158935 158939 158941 158943 158944 158945 158947 158948 158949 158951 158953 158957 158959 158963 158965 158969 158975 158977 158983 158987 158989 158993 158999 159005 159007 159013 159017 159019 159025 159029 159035 159043 203614
| A. | 高纯硅可用于制造光导纤维 | |
| B. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 | |
| C. | 硅的化学性质不活泼,在自然界中可以以游离态存在 | |
| D. | 硅在电子工业中,是重要的半导体材料 |
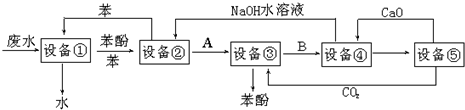
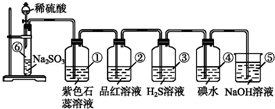
 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H 6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H 6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
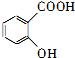 .
. .
. )为主要原料
)为主要原料 制备合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$
制备合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$ .
.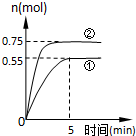 碳循环的途径之一是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ,在容积为2L的密闭容器中充入1mol CO2和3mol H2,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如图所示:
碳循环的途径之一是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ,在容积为2L的密闭容器中充入1mol CO2和3mol H2,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如图所示: 人体中含量位于前6名的元素依次是:氢、氧、X、氮、钙、磷.根据要求用以上元素完成下列填空:
人体中含量位于前6名的元素依次是:氢、氧、X、氮、钙、磷.根据要求用以上元素完成下列填空: ;该分子的空间构型为正四面体结构.
;该分子的空间构型为正四面体结构.