12.氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
(1)根据下面能量变化示意图(图1),请写出 NO 和 CO2 反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.

(2)在固定体积的密闭容器中,进行如下化学反应:2NH3(g)?N2(g)+3H2(g)△H>0,其平衡常数 K 与温度 T 的关系如表:
①试判断 K1<K2(填写“>”,“<”或“=”);
②该反应的熵变△S>0 (填“>”,“<”或“=”);
③下列各项能说明该反应已达到平衡状态的是c(填字母);
a.容器内 N2、H2、NH3 的物质的量之比为 1:3:2
b.2v(NH3)正=3v(H2)
c.容器内混合气体平均相对分子质量保持不变
d.混合气体的密度保持不变
④一定温度下,在 1L 密闭容器中充入 1molN2 和 3molH2 并发生反应.若容器容积恒 定,10min 达到平衡时,气体的总物质的量为原来的$\frac{9}{10}$,则 N2 的转化率 α(N2)=20%.
(3)在常温常压下 pH 均等于 5 的 CH3COOH 和 HCl 溶液,两种溶液中由水电离出来的c(H+)之比为1:1.
(4)对反应 N2O4(g)?2NO2(g)△H>0,在温度分别为 T1、T2时,平衡体 系中 NO2 的体积分数随压强变化曲线如图2所示,下列说法正确的是cd.
a.A、C 两点的反应速率:A>C
b.A、C 两点的化学平衡常数:A>C
c.A、C 两点 N2O4 的转化率:A>C
d.由状态 B 到状态 A,可以用加热的方法.
(1)根据下面能量变化示意图(图1),请写出 NO 和 CO2 反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.

(2)在固定体积的密闭容器中,进行如下化学反应:2NH3(g)?N2(g)+3H2(g)△H>0,其平衡常数 K 与温度 T 的关系如表:
| T/K | 2.98 | 398 | 498 |
| 平衡常数K | 2.44×10-6 | K1 | K2 |
②该反应的熵变△S>0 (填“>”,“<”或“=”);
③下列各项能说明该反应已达到平衡状态的是c(填字母);
a.容器内 N2、H2、NH3 的物质的量之比为 1:3:2
b.2v(NH3)正=3v(H2)
c.容器内混合气体平均相对分子质量保持不变
d.混合气体的密度保持不变
④一定温度下,在 1L 密闭容器中充入 1molN2 和 3molH2 并发生反应.若容器容积恒 定,10min 达到平衡时,气体的总物质的量为原来的$\frac{9}{10}$,则 N2 的转化率 α(N2)=20%.
(3)在常温常压下 pH 均等于 5 的 CH3COOH 和 HCl 溶液,两种溶液中由水电离出来的c(H+)之比为1:1.
(4)对反应 N2O4(g)?2NO2(g)△H>0,在温度分别为 T1、T2时,平衡体 系中 NO2 的体积分数随压强变化曲线如图2所示,下列说法正确的是cd.
a.A、C 两点的反应速率:A>C
b.A、C 两点的化学平衡常数:A>C
c.A、C 两点 N2O4 的转化率:A>C
d.由状态 B 到状态 A,可以用加热的方法.
11.在某无色、透明的强酸性溶液中,能大量共存的离子组是( )
| A. | NH4+、NO3-、Al3+、Cl- | B. | K+、SO42-、Ba2+、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | H+、SO42-、HCO3-、Na+ |
9.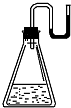 有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )
有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )
 有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )
有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )| A. | ①②③④ | B. | ①②④ | C. | ②③④ | D. | ①②③ |
7.下列有关化学用语表达不正确的是( )
| A. | 二氧化碳的结构式:O=C=O | B. | 氯离子的结构示意图: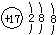 | ||
| C. | 钙离子的电子式:Ca2+ | D. | 溴化氢分子的电子式: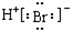 |
6.下列过程中化学键未被破坏的是( )
0 158837 158845 158851 158855 158861 158863 158867 158873 158875 158881 158887 158891 158893 158897 158903 158905 158911 158915 158917 158921 158923 158927 158929 158931 158932 158933 158935 158936 158937 158939 158941 158945 158947 158951 158953 158957 158963 158965 158971 158975 158977 158981 158987 158993 158995 159001 159005 159007 159013 159017 159023 159031 203614
| A. | NaCl固体溶于水 | B. | NH4Cl受热分解 | C. | 干冰升华 | D. | SO2气体溶于水 |
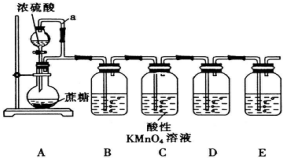
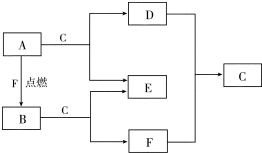 A、D、F均是由短周期元素组成的单质,常温下C是液体.
A、D、F均是由短周期元素组成的单质,常温下C是液体.
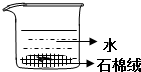
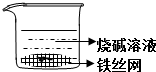
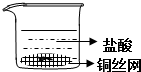
 磷是生物体中不可缺少的元素之一,它能形成多种化合物.
磷是生物体中不可缺少的元素之一,它能形成多种化合物.