13.在常温下,纯水中存在电离平衡H2O?H++OH-,如果要使水的电离程度增大,并使c(H+)增大,应加入的物质是( )
| A. | NaHSO4 | B. | KAl(SO4)2 | C. | NaHCO3 | D. | CH3COONa |
12.将0.1mol/L的醋酸钠溶液20ml与0.1mol/L盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
| A. | c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH)>c(OH-) | |
| C. | c(CH3 COO-)=c(Cl-)>c(H+)>c(CH3COOH)>c(OH-) | |
| D. | c(Cl-)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
11.下列文字表述与离子方程式对应且正确的是( )
| A. | 用石墨作电极电解NaCl溶液:2C1-+2H2O$\frac{\underline{\;电解\;}}{\;}$C12↑+2OH-+H2↑ | |
| B. | 硫氢化钠的水解:HS-+H2O?H3O++S2- | |
| C. | 硫化钠的水解:S2-+2H2O?H2S+2OH- | |
| D. | 碳酸氢钠与氢氧化钠溶液的反应:HCO3-+OH-=CO32-+H2O |
10.氯气和二氧化硫都可以做漂白剂,若两者混合使用,漂白效果会( )
| A. | 增强 | B. | 减弱 | C. | 不变 | D. | 难以确定 |
9.一定温度下,向 a L密闭容器中加入1mol X 气体和2mol Y 气体,发生如下反应:X(g)+2Y(g)?3Z(g),此反应达到平衡的标志是( )
| A. | 容器内压强不再随时间变化 | |
| B. | 单位时间内消耗0.1 mol X 的同时生成0.3 molZ | |
| C. | 容器内XYZ的浓度比为1:2:3 | |
| D. | 容器内各物质浓度不再随时间变化 |
8.物质结构理论推出:金属晶体中金属离子与自由电子之间的强烈相互作用,叫金属键.金属键越强,其金属的硬度越大,熔沸点越高,且据研究表明,一般说来金属原子半径越小,价电子数越多,则金属键越强,由此判断下列说法错误的是( )
| A. | 钠的硬度大于铝 | B. | 镁的熔沸点高于钙 | ||
| C. | 镁的硬度大于钾 | D. | 钙的熔沸点高于钾 |
7.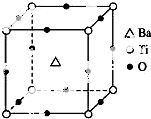 如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
 如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )| A. | 8 BaTi8O12 | B. | 8 BaTi4O9 | C. | 6 BaTiO3 | D. | 3 BaTi2O3 |
6.下列反应中,属于取代反应的是( )
| A. | CH4+2O2$\stackrel{点燃}{→}$ CO2+2H2O | B. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | ||
| C. | CH4$\stackrel{高温}{→}$ C+2H2 | D. | 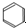 +HO-NO2$→_{△}^{浓硫酸}$H2O+ +HO-NO2$→_{△}^{浓硫酸}$H2O+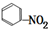 |
5.有一混合物水溶液,可能含有以下离子中的若干种:K+、NH4+、Cl-、Fe3+、Mg2+、CO32-、SO42-,现各取100mL溶液三份进行实验.
(1)向第一份加入AgNO3溶液,有白色沉淀产生;
(2)向第二份加入足量NaOH溶液后加热,收集气体0.896L(标准状况);
(3)向第三份加入足量的BaCl2溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g.
试回答下列问题:
(1)肯定存在的离子有K+、NH4+、CO32-、SO42-,肯定不存在的离子有Fe3+、Mg2+.
(2)可能存在的离子是Cl-,为确定该离子是否存在,可取少许原试液,然后加入足量的稀硝酸和硝酸钡溶液,过滤,向滤液中滴入AgNO3溶液,若有白色沉淀生成,则证明有Cl-存在(填实验操作).
(3)试分别确定肯定存在的离子在原溶液中各自的物质的量浓度:
(1)向第一份加入AgNO3溶液,有白色沉淀产生;
(2)向第二份加入足量NaOH溶液后加热,收集气体0.896L(标准状况);
(3)向第三份加入足量的BaCl2溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g.
试回答下列问题:
(1)肯定存在的离子有K+、NH4+、CO32-、SO42-,肯定不存在的离子有Fe3+、Mg2+.
(2)可能存在的离子是Cl-,为确定该离子是否存在,可取少许原试液,然后加入足量的稀硝酸和硝酸钡溶液,过滤,向滤液中滴入AgNO3溶液,若有白色沉淀生成,则证明有Cl-存在(填实验操作).
(3)试分别确定肯定存在的离子在原溶液中各自的物质的量浓度:
| 离子 | 物质的量浓度 |
| NH4+ | 0.4mol•L-1 |
| CO32- | 0.2mol•L-1 |
| SO42- | 0.1mol•L-1 |
| K+ | -≥0.2mol/l |
4.根据图,下列判断中正确的是( )

0 158827 158835 158841 158845 158851 158853 158857 158863 158865 158871 158877 158881 158883 158887 158893 158895 158901 158905 158907 158911 158913 158917 158919 158921 158922 158923 158925 158926 158927 158929 158931 158935 158937 158941 158943 158947 158953 158955 158961 158965 158967 158971 158977 158983 158985 158991 158995 158997 159003 159007 159013 159021 203614

| A. | 该装置将电能转化为化学能 | B. | Fe电极发生了氧化反应 | ||
| C. | 烧杯a中的溶液pH降低 | D. | 烧杯b中发生的反应为Zn-2e-=Zn2+ |