5.下列影响化学反应速率的因素中,是通过改变活化分子百分数来实现的是( )
①改变气体物质的浓度 ②改变气体的压强
③加入催化剂 ④改变气体的温度.
①改变气体物质的浓度 ②改变气体的压强
③加入催化剂 ④改变气体的温度.
| A. | 只有①② | B. | 只有③④ | C. | 只有①③④ | D. | ①②③④ |
4.利用电解法可将Fe、Zn、Ag、Au等杂质的粗铜提纯,下列叙述正确的是( )
| A. | 电解时以纯铜作阳极 | |
| B. | 电解时阳极发生还原反应 | |
| C. | 纯铜连接电源负极,电极反应是Cu-2e-=Cu2+ | |
| D. | 电解后,电解槽底部会形成含少量Ag、Au等金属阳极泥 |
2.下列有关实验操作的“先”与“后”的说法中,正确的是( )
| A. | 制取气体时,先装药品,后检查装置的气密性 | |
| B. | 加热KClO3并用排水法收集O2实验结束时,先熄灭酒精灯,后移出导管 | |
| C. | 稀释浓硫酸时,先把浓硫酸倒入烧杯中,后沿器壁缓慢注入水,边加边搅拌 | |
| D. | 加热试管时,先使试管底部均匀受热,后用酒精灯的外焰固定加热 |
1.下列化学方程式书写正确的是( )
| A. | Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | B. | 3Cu+8HO3(浓)=3Cu(NO3)2+2NO↑+4H2O | ||
| C. |  | D. | 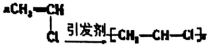 |
20.在同温同压下,下列各组热化学方程式中△H1>△H2的是( )
| A. | 2H2(g)+O2(g)═2H2O(l);△H1 2H2(g)+O2(g)═2H2O(g);△H2 | |
| B. | S(g)+O2(g)═2SO2(g);△H1 S(s)+O2(g)═2SO2(g);△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g);△H1 C(s)+O2(g)═CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g);△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g);△H2 |
18.随着卤素原子核电荷数的递增,下列递变规律正确的是( )
| A. | 单质的熔沸点逐渐升高 | B. | 氢化物的稳定性逐渐增强 | ||
| C. | 单质的氧化性逐渐增强 | D. | 元素的非金属性逐渐增强 |
17.在短周期元素中,属于金属元素的有( )
0 158812 158820 158826 158830 158836 158838 158842 158848 158850 158856 158862 158866 158868 158872 158878 158880 158886 158890 158892 158896 158898 158902 158904 158906 158907 158908 158910 158911 158912 158914 158916 158920 158922 158926 158928 158932 158938 158940 158946 158950 158952 158956 158962 158968 158970 158976 158980 158982 158988 158992 158998 159006 203614
| A. | 13种 | B. | 9种 | C. | 5种 | D. | 3种 |

 .
. .
. ,元素D在元素周期表中的位置是第三周期VIIA族.
,元素D在元素周期表中的位置是第三周期VIIA族.