5.为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | CH3CH2OH (CH3COOH) | CaO | 蒸馏 |
| D | CH3COOC2H5 (CH3COOH) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
4.下列指定微粒的数目相等的是( )
| A. | 等物质的量的CaCl2和CaO2含有的离子数 | |
| B. | 等温等压下,质子数相等的CO、N2、C2H2三种气体含有的原子数 | |
| C. | 同温、同压、同体积的CO和NO含有的质子数 | |
| D. | 物质的量相同的铁和铝分别与足量氯气完全反应时转移的电子数 |
3.在氧化还原反应的过程中,氧化反应和还原反应同时发生,下列有关SO2-2e-+2H2O→SO42-+4H+的说法正确的是( )
| A. | 该反应为还原反应 | |
| B. | 上述反应中若产生0.1mol SO42-,则消耗SO2的物质的量为0.1mol | |
| C. | Fe2(SO4)3、品红两种溶液都能使上述反应进行 | |
| D. | 通入Cl2会增强SO2的漂白作用 |
2.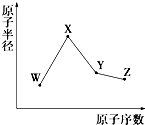 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料.Z的非金属性在同周期元素中最强.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料.Z的非金属性在同周期元素中最强.下列说法正确的是( )
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料.Z的非金属性在同周期元素中最强.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料.Z的非金属性在同周期元素中最强.下列说法正确的是( )| A. | 对应简单离子半径:X>W | |
| B. | 对应气态氢化物的稳定性:Y>Z | |
| C. | 化合物XZW既含离子键,又含共价键,属于弱电解质 | |
| D. | Y的氧化物和Z的氢化物均能与X的最高价氧化物对应的水化物反应 |
1.下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
20.某同学用回收的镁铝合金制取氢气.现有10.8g镁铝合金,下列说法正确的是( )
| A. | 常温下与足量18mol/LH2SO4反应,最多可放出0.6molH2 | |
| B. | 常温下与足量2mol/LHNO3反应,最少可放出0.45molH2 | |
| C. | 常温下与足量2mol/LH2SO4反应,放出H2的量在0.45mol~0.6mol之间 | |
| D. | 常温下与足量2mol/LNaOH反应,放出H2的量在0.45mol~0.6mol之间 |
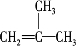
18.化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷.若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
| A. | CH3CH2CH2CH2CH2OH | B. | (CH3)2COHCH2CH3 | ||
| C. | (CH3)2CHCH2CH2OH | D. | (CH3)3CCH2OH |
17.用水能鉴别的一组物质是( )
0 158810 158818 158824 158828 158834 158836 158840 158846 158848 158854 158860 158864 158866 158870 158876 158878 158884 158888 158890 158894 158896 158900 158902 158904 158905 158906 158908 158909 158910 158912 158914 158918 158920 158924 158926 158930 158936 158938 158944 158948 158950 158954 158960 158966 158968 158974 158978 158980 158986 158990 158996 159004 203614
| A. | 乙醇和乙酸 | B. | 乙酸乙酯和乙醇 | C. | 苯和乙酸乙酯 | D. | 四氯化碳和溴苯 |
 .
.