12.某些保健品中含有的锗元素(Ge)位于周期表的第四周期IVA族.有关锗的叙述不正确的是( )
| A. | 锗的原子序数为24 | B. | 锗的金属活动性应比硅强 | ||
| C. | Ge可以生成化学式为Na2GeO3的盐 | D. | 单质锗是半导体材料 |
11.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1mol氦气中含有2NA个氦原子 | |
| B. | 14g氮气中含有NA个氮原子(氮的相对原子质量为14) | |
| C. | 46g NO2中含有氧原子2NA | |
| D. | 18g水中所含有的电子数为8NA |
10.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 12g金刚石含有的共价键数为4NA | |
| B. | 1.00molNaCl中约含有6.02×1023个NaCl分子 | |
| C. | 常温下,23g NO2和N2O4的混合物含有1.5NA个原子 | |
| D. | agC2H4和C3H6的混合物所含共用电子对数目为($\frac{a}{7}$+1)NA |
9.T℃时在2L恒容密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.下列说法错误的是( )


| A. | 容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) | |
| B. | 保持其他条件不变,升高温度,反应的化学平衡常数K减小 | |
| C. | 反应进行的前3 min内,用X表示的反应速率 v(X)=0.2mol•(L•min)-1 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
8.合成氨反应:3H2+N2=2NH3其反应速率可以分别用v(H2)、v(N2)、v(NH3)[单位均为mol/(L•s)]表示,则正确的关系是( )
| A. | v(H2)=v(N2)=v(NH3) | B. | v(H2)=v(NH3) | C. | 2v(N2)=v(NH3) | D. | v(N2)=3v(H2) |
7.用下列实验装置进行相应实验,能达到实验目的是( )
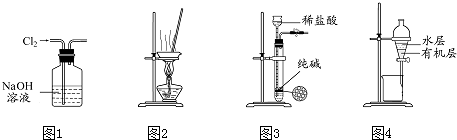

| A. | 用图1 所示装置除去Cl2中含有的少量HCl | |
| B. | 用图2 所示装置蒸干NH4HCO3饱和溶液制备NH4HCO3晶体 | |
| C. | 用图3 所示装置制取少量纯净的CO2气体 | |
| D. | 用图4 所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
6.下列有关实验操作的说法正确的是( )
| A. | 可用25mL碱式滴定管量取20.00mL KMnO4溶液 | |
| B. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| C. | 向煮沸的1 mol/L NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体 | |
| D. | 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的$\frac{2}{3}$,液体也不能蒸干 |
5.为证明化学反应有一定的限度,进行如下探究活动:I.取5m1 0.1mol/L的KI溶液,滴加几滴FeCl3稀溶液(已知:2Fe3++2I-=I2+2Fe2+)Ⅱ.继续加入2ml CCl4振荡.Ⅲ.取萃取后的上层清液,滴加KSCN溶液.
(1)探究活动I的实验现象为溶液呈棕黄色;探究活动Ⅱ的实验现象为溶液分层,下层CCl4层呈紫红色.
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+;
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大,Fe(SCN)3在乙醚中与在水中呈现的颜色相同;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6](黄色)溶液检验Fe3+的灵敏度比用KSCN更高.结合新信息,现设计以下实验方案验证猜想:
ⅰ.请完成下表实验操作、现象和结论
ⅱ.写出实验操作“步骤一”中反应的离子方程式为4Fe3++3[Fe(CN)6]4-═Fe4[Fe(CN)6]3↓..
(1)探究活动I的实验现象为溶液呈棕黄色;探究活动Ⅱ的实验现象为溶液分层,下层CCl4层呈紫红色.
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+;
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大,Fe(SCN)3在乙醚中与在水中呈现的颜色相同;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6](黄色)溶液检验Fe3+的灵敏度比用KSCN更高.结合新信息,现设计以下实验方案验证猜想:
ⅰ.请完成下表实验操作、现象和结论
| 实 验 操 作 | 现 象 和 结 论 |
| 步骤一:取萃取后的上层清液滴加2滴K4[Fe(CN)6] | 若产生①蓝色沉淀, 则②猜想一不成立; |
| 步骤二:往探究Ⅲ所得溶液中加入少量乙醚,充分振荡、静置分层 | 若③乙醚层呈血红色, 则④猜想二成立; |
4.下列反应的离子方程式不正确的是( )
| A. | 大理石与醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| B. | 硅与NaOH溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ | |
| C. | 水玻璃与醋酸反应:SiO32-+2H+═H2SiO3↓ | |
| D. | 硅石与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
3.将10g碳酸钙固体高温煅烧一段时间,冷却后投入足量的稀盐酸中完全反应.有关结论错误的是( )
0 158798 158806 158812 158816 158822 158824 158828 158834 158836 158842 158848 158852 158854 158858 158864 158866 158872 158876 158878 158882 158884 158888 158890 158892 158893 158894 158896 158897 158898 158900 158902 158906 158908 158912 158914 158918 158924 158926 158932 158936 158938 158942 158948 158954 158956 158962 158966 158968 158974 158978 158984 158992 203614
| A. | 共生成0.1mol氧化钙 | |
| B. | 煅烧越充分则消耗的盐酸越少 | |
| C. | 共生成0.1mol二氧化碳 | |
| D. | 煅烧后固体中氧元素的质量分数减小 |