11.在某密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,针对图象下列分析不正确的是( )


| A. | 图Ⅰ研究的是t1时刻增大压强(缩小体积)对反应速率的影响 | |
| B. | 图Ⅱ研究的是t1时刻通入氦气(保持恒容)对反应速率的影响 | |
| C. | 图Ⅱ研究的是t1时刻加入正催化剂对反应速率的影响 | |
| D. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
10.等质量的SO2和SO3相比较,下列正确的是( )
| A. | 它们的分子数目之比为1:1 | B. | 它们的氧原子数目之比为4:5 | ||
| C. | 它们的体积之比为5:4 | D. | 它们所含的硫原子数之比为5:4 |
8.在容积不变的密闭容器中加入1mol N2和3mol H2反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,下列结论正确的是( )
| A. | 该反应达到平衡时,放出的热量等于92.4kJ | |
| B. | 达到平衡后向容器中通入1mol氦气,容器内压强增大,平衡向右移动 | |
| C. | 降低温度和缩小容器体积均可使该反应的平衡常数增大 | |
| D. | 若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的90% |
7. 实验室利用如图装置进行中和热的测定,请回答下列问题:
实验室利用如图装置进行中和热的测定,请回答下列问题:
(1)从实验装置上看,图中尚缺少的玻璃用品是环形玻璃搅拌棒.
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果;
(3)做一次完整的中和热测定实验,温度计需使用3次;
(4)把温度为13℃,浓度为1.0mol/L的酸溶液和1.1mol/L的碱溶液各50mL混合[溶液密度均为1g/mL,生成溶液的比热容c=4.184J/(g•°C)],轻轻搅动,测得酸碱混合液的温度变化数据如表:
①计算上述两组实验测出的中和热:提示$△H=-\frac{{0.4184({t_2}-{t_1})}}{{n({H_2}O)}}kJ/mol$2△H1=-56.9kJ/mol;
△H2=-52.7kJ/mol.
②两组实验结果差异的原因是一水合氨为弱碱,在中和过程中一水合氨发生电离,要吸收热量,因而总体放热较少.
 实验室利用如图装置进行中和热的测定,请回答下列问题:
实验室利用如图装置进行中和热的测定,请回答下列问题:(1)从实验装置上看,图中尚缺少的玻璃用品是环形玻璃搅拌棒.
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果;
(3)做一次完整的中和热测定实验,温度计需使用3次;
(4)把温度为13℃,浓度为1.0mol/L的酸溶液和1.1mol/L的碱溶液各50mL混合[溶液密度均为1g/mL,生成溶液的比热容c=4.184J/(g•°C)],轻轻搅动,测得酸碱混合液的温度变化数据如表:
| 反应物 | 起始温度t1/°C | 终了温度t2/°C | 中和热 |
| HCl+NaOH | 13 | 19.8 | △H1 |
| HCl+NH3•H2O | 13 | 19.3 | △H2 |
△H2=-52.7kJ/mol.
②两组实验结果差异的原因是一水合氨为弱碱,在中和过程中一水合氨发生电离,要吸收热量,因而总体放热较少.
6.在4L密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),达到平衡时,生成了2mol C,经测定,D的浓度为0.5mol•L-1,下列判断正确的是( )
| A. | B的转化率为20% | |
| B. | 平衡时A的浓度为1.50 mol•L-1 | |
| C. | x=1 | |
| D. | 达到平衡时,在相同温度下容器内混合气体的压强是反应前的85% |
4.目前,由化学能转变为热能或电能仍是人类使用的最主要能源.
I.氢气是一种很有前途的新能源,以水为原料大量制取氢气的最理想途径是a.
a.利用太阳能直接将水分解产生氢气 b.以焦炭和水制取水煤气后分离出氢气
c.用Fe跟HCl反应放出氢气 d.由热电站提供电力电解水产生氢气
II.下表列出了断裂1mol某些化学键所需的能量
已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,回答下列问题:
(1)该反应属于_放热(填“放热”或“吸热”)反应,1mol H2(g)和0.5molO2(g)的总能量大于(填“大于”“小于”或“等于”) 1mol H2O(g)的总能量,此反应中化学能主要转化为热能.
(2)表中a=496.4 kJ.
(3)若H2O(l)═H2O(g)△H=+44kJ•mol-1
请写出H2(g)燃烧生成液态水时的热化学方程式_H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1.
0 158784 158792 158798 158802 158808 158810 158814 158820 158822 158828 158834 158838 158840 158844 158850 158852 158858 158862 158864 158868 158870 158874 158876 158878 158879 158880 158882 158883 158884 158886 158888 158892 158894 158898 158900 158904 158910 158912 158918 158922 158924 158928 158934 158940 158942 158948 158952 158954 158960 158964 158970 158978 203614
I.氢气是一种很有前途的新能源,以水为原料大量制取氢气的最理想途径是a.
a.利用太阳能直接将水分解产生氢气 b.以焦炭和水制取水煤气后分离出氢气
c.用Fe跟HCl反应放出氢气 d.由热电站提供电力电解水产生氢气
II.下表列出了断裂1mol某些化学键所需的能量
| 化学键 | H-H | O=O | O-H |
| 能量(kJ) | 436 | a | 463 |
(1)该反应属于_放热(填“放热”或“吸热”)反应,1mol H2(g)和0.5molO2(g)的总能量大于(填“大于”“小于”或“等于”) 1mol H2O(g)的总能量,此反应中化学能主要转化为热能.
(2)表中a=496.4 kJ.
(3)若H2O(l)═H2O(g)△H=+44kJ•mol-1
请写出H2(g)燃烧生成液态水时的热化学方程式_H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1.
 已知六方氮化硼类似于石墨的结构,如图所示,利用所学知识结合该图回答下列问题.
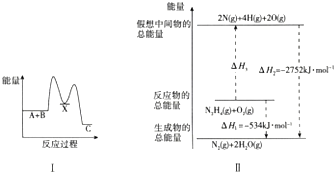
已知六方氮化硼类似于石墨的结构,如图所示,利用所学知识结合该图回答下列问题. 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.