19.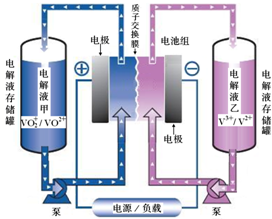 (1)全钒液流电池储能技术及应用荣获2015年国家技术发明二等奖.其结构及工作原理如图所示,电解液均呈酸性.
(1)全钒液流电池储能技术及应用荣获2015年国家技术发明二等奖.其结构及工作原理如图所示,电解液均呈酸性.
①该电池放电时,正极反应为VO2++2H++e-═VO2++H2O,充电的总反应方程式为V3++VO2++H2O=VO2++2H++V2+.
②用该电池做电源,电解精炼铜,当外电路中通过1mol电子时,通过质子交换膜的n(H+)=1mol,析出铜的质量为32g.
(2)已知25℃时三种酸的电离常数如表所示:
①等浓度的NaCN溶液、CH3COONa溶液和Na2CO3溶液,溶液的pH由大到小的顺序为:Na2CO3>NaCN>CH3COONa(填化学式).
②在0.5mol•L-1的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的9×108倍.
 (1)全钒液流电池储能技术及应用荣获2015年国家技术发明二等奖.其结构及工作原理如图所示,电解液均呈酸性.
(1)全钒液流电池储能技术及应用荣获2015年国家技术发明二等奖.其结构及工作原理如图所示,电解液均呈酸性.①该电池放电时,正极反应为VO2++2H++e-═VO2++H2O,充电的总反应方程式为V3++VO2++H2O=VO2++2H++V2+.
②用该电池做电源,电解精炼铜,当外电路中通过1mol电子时,通过质子交换膜的n(H+)=1mol,析出铜的质量为32g.
(2)已知25℃时三种酸的电离常数如表所示:
| 化学式 | 电离常数 |
| HCN | K=6.2×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
②在0.5mol•L-1的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的9×108倍.
18.55g铁铝混合物与足量的盐酸反应生成标准状况下的氢气44.8L,则混合物中铁和铝的物质的量之比为( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 2:3 |
17.取pH值均等于2的盐酸和醋酸各100ml分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A. | 醋酸与锌反应放出氢气多 | |
| B. | 从反应开始到结束所需时间盐酸短 | |
| C. | 醋酸与锌反应速率大 | |
| D. | 盐酸和醋分别与锌反应的速度一样大 |
16.有如图反应:mA(g)?nB(g),当加压后,反应速率如图所示,推断系数m和n的关系是( )

| A. | m>n | B. | m<n | C. | m=n | D. | 无法确定 |
14.能将乙烷、乙烯两种气体鉴别出来的试剂是( )
| A. | 溴水 | B. | KMnO4溶液 | C. | 酒精 | D. | 水 |
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L的CCl4中含CCl4分子数为NA | |
| B. | 5.6g 铁和6.4g 铜分别与0.1mol 氯气完全反应,转移的电子数相等 | |
| C. | 0.1mol•L-1MgCl2溶液中含Cl-数为0.2NA | |
| D. | 3.9g Na2O2晶体中含有的离子总数为0.2NA |
11.下列离子方程式书写正确的是( )
0 158781 158789 158795 158799 158805 158807 158811 158817 158819 158825 158831 158835 158837 158841 158847 158849 158855 158859 158861 158865 158867 158871 158873 158875 158876 158877 158879 158880 158881 158883 158885 158889 158891 158895 158897 158901 158907 158909 158915 158919 158921 158925 158931 158937 158939 158945 158949 158951 158957 158961 158967 158975 203614
| A. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | 钠与水的反应Na+2H2O=Na++2OH-+H2↑ | |
| C. | 铜片跟稀硝酸反应:Cu+NO3-+4H+═Cu2++NO↑+2H2O | |
| D. | 铝片和氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |