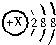19.某废水中可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2一、CO32-、S2一、SO32-、SO42-现取该溶液进行有关实验,实验过程及现象如下:下列说法正确的是( )
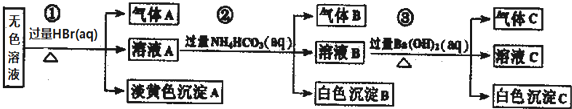

| A. | 根据实验①中的现象可推出,气体A一定是纯净物,淡黄色沉淀一定是AgBr | |
| B. | 根据实验②中的现象可推出,气体B是CO2,沉淀B是Al(OH)3,原溶液中一定含有Al3+ | |
| C. | 根据实验③中的现象可推出,气体C是NH3,沉淀C一定有BaCO3,可能有BaSO4 | |
| D. | 原溶液中肯定含有Na+、AlO2-、S2-,不能确定是否含有SO32-、SO42- |
16. 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶 液进行中和热的测定,实验装置如图所示.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶 液进行中和热的测定,实验装置如图所示.
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和环形玻璃搅拌棒
(2)写出该反应的热化学方程式(中和热为57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
(3)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-53.5kJ/mol (取小数点后一位).
(4)如果用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,中和热实验数值偏低.(填“偏高”,“无影响”或“偏低”)
 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶 液进行中和热的测定,实验装置如图所示.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶 液进行中和热的测定,实验装置如图所示. (1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和环形玻璃搅拌棒
(2)写出该反应的热化学方程式(中和热为57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
(3)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 |
| 2 | 25.9 | 25.9 | 25.9 | 29.8 |
| 3 | 26.4 | 26.2 | 26.3 | 30.4 |
(4)如果用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,中和热实验数值偏低.(填“偏高”,“无影响”或“偏低”)
15.下列实验不能做为判断依据的是( )
| A. | 根据钠和镁分别与冷水的反应情况,判断钠和镁金属性的强弱 | |
| B. | 根据氯水与溴化钠溶液的反应情况,判断氯和溴非金属性的强弱 | |
| C. | 根据HF和HCl的水溶液的酸性强弱,判断氟与氯非金属的强弱 | |
| D. | 根据Na+和K+的氧化性的强弱,判断钠和钾的金属性的强弱 |
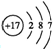
13.在第n层电子层中,当它作为原子的最外电子层时,容纳电子数最多与第(n-1)层相同;当它作为原子的次外电子层时,其电子数比第(n-1)层多10个,则对此电子层的判断正确的是( )
| A. | 必为第1层 | B. | 只能是第2层 | C. | 只能是第3层 | D. | 可以是任意层 |
11.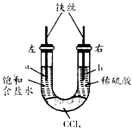 利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间.下列说法正确的是( )
利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间.下列说法正确的是( )
0 158769 158777 158783 158787 158793 158795 158799 158805 158807 158813 158819 158823 158825 158829 158835 158837 158843 158847 158849 158853 158855 158859 158861 158863 158864 158865 158867 158868 158869 158871 158873 158877 158879 158883 158885 158889 158895 158897 158903 158907 158909 158913 158919 158925 158927 158933 158937 158939 158945 158949 158955 158963 203614
 利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间.下列说法正确的是( )
利用如图装置进行实验,开始时,左右两管液面相平,密封好,放置一段时间.下列说法正确的是( )| A. | 左管中O2得到电子,右管中H+得到电子 | |
| B. | 一段时间后,左管液面低于右管液面 | |
| C. | a、b两处具有相同的电极反应式:Fe-3e-=Fe3+ | |
| D. | a处溶液的pH增大,b处溶液的pH减小 |
 ,B中所含的化学键有离子键、共价键.又知X溶液显碱性,其原因是(用离子方程式表示)ClO-+H2O?HClO+OH-.
,B中所含的化学键有离子键、共价键.又知X溶液显碱性,其原因是(用离子方程式表示)ClO-+H2O?HClO+OH-.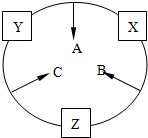 原子序数之和为16的三种短周期元素x、y、z对应的单质 X、Y、Z,常温常压下均为无色气体,在适当条件下单质X、Y、Z之间可以发生如图所示的变化.已知B分子组成中z原子个数比C分子中少一个.
原子序数之和为16的三种短周期元素x、y、z对应的单质 X、Y、Z,常温常压下均为无色气体,在适当条件下单质X、Y、Z之间可以发生如图所示的变化.已知B分子组成中z原子个数比C分子中少一个. .
.