19.下列处理不正确的是( )
| A. | 苯酚沾在手上立即用酒精清洗 | B. | 误食铜盐立即喝牛奶或蛋清 | ||
| C. | 动物标本可用福尔马林浸泡防腐 | D. | 伤口处理应先用100%的乙醇消毒 |
18.如图各容器中盛有稀硫酸,能形成原电池且铁为负极的是( )
| A. |  | B. |  | C. |  | D. |  |
13.下列关于化学键的说法正确的是( )
| A. | 化学键既存在于相邻原子之间,又存在与相邻分子之间 | |
| B. | 非极性键只存在于双原子的单质分子中 | |
| C. | 相邻原子之间的强相互作用 | |
| D. | 共价键只能存在于共价化合物中 |
12.关于如图各装置图的叙述不正确的是( )
| A. | 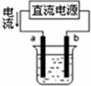 用如图装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 | |
| B. | 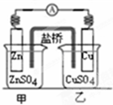 如图装置的盐桥中KCl的Cl-移向乙烧杯 | |
| C. |  如图装置中钢闸门应与外接电源的负极相连获得保护 | |
| D. | 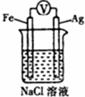 装置中滴入2滴黄色K3[Fe(CN)6]溶液,溶液中可能出现蓝色沉淀 |
11.氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色.下图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:

根据以上信息回答下列问题:
(1)写出生产过程中XFe Y稀盐酸(填化学式).
(2)写出产生CuCl的化学方程式CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,所以理论上不需要补充SO2气体.
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题是防止CuCl的氧化和见光分解,减少产品CuCl的损失.
(5)实验探究pH对CuCl产率的影响如表所示:
析出CuCl晶体最佳pH为2,当pH较大时CuCl产率变低原因是pH较大时,Cu2+水解程度增大,反应生成CuCl减少,产率减小.
(6)氯化亚铜的定量分析:
①称取样品0.25g和10mL过量的FeCl3溶液250mL于锥形瓶中,充分溶解.
②用0.10mol•L-1硫酸铈标准溶液滴定.已知:CuCl+FeCl3═CuCl2+FeCl2;Fe2++Ce4+═Fe3++Ce3+.三次平行实验结果如表(平行实验结果相差不能超过1%):
则样品中CuCl的纯度为95.5%(结果保留三位有效数字).
0 158767 158775 158781 158785 158791 158793 158797 158803 158805 158811 158817 158821 158823 158827 158833 158835 158841 158845 158847 158851 158853 158857 158859 158861 158862 158863 158865 158866 158867 158869 158871 158875 158877 158881 158883 158887 158893 158895 158901 158905 158907 158911 158917 158923 158925 158931 158935 158937 158943 158947 158953 158961 203614

根据以上信息回答下列问题:
(1)写出生产过程中XFe Y稀盐酸(填化学式).
(2)写出产生CuCl的化学方程式CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,所以理论上不需要补充SO2气体.
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题是防止CuCl的氧化和见光分解,减少产品CuCl的损失.
(5)实验探究pH对CuCl产率的影响如表所示:
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率 | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
(6)氯化亚铜的定量分析:
①称取样品0.25g和10mL过量的FeCl3溶液250mL于锥形瓶中,充分溶解.
②用0.10mol•L-1硫酸铈标准溶液滴定.已知:CuCl+FeCl3═CuCl2+FeCl2;Fe2++Ce4+═Fe3++Ce3+.三次平行实验结果如表(平行实验结果相差不能超过1%):
| 平行实验次数 | 1 | 2 | 3 |
| 0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |

 CH3COOCH(CH3)2+H2O,取代反应或酯化反应反应类型
CH3COOCH(CH3)2+H2O,取代反应或酯化反应反应类型


 元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(如图,其它参与反应的物质未列出):
元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(如图,其它参与反应的物质未列出): .
.