6.某化学兴趣小组为探究卤族元素中氯、溴、碘的非金属性强弱,进行了如下实验,完成下表:
由以上结论可知,三种元素的非金属性由强到弱的顺序是Cl>Br>I.
| 实验操作 | 实验现象 | 离子方程式 | 单质氧化性 |
| 向NaBr溶液中滴入氯水,一段时间后再加入CCl4 | 静置后,液体分层,上层接近无色,下层橙红色 | 2Br-+Cl2=2 Cl-+Br2 | Cl2>Br2 |
| 向KI溶液中滴入氯水,一段时间后再加入CCl4 | 静置后,液体分层,上层接近无色,下层紫色 | 2I-+Cl2=2 Cl-+I2 | Cl2>I2 |
| 向KI溶液中滴入溴水,一段时间后再加入CCl4 | 静置后,液体分层,上层接近无色,下层紫色 | 2I-+Br2=2 Br-+I2 | Br2>I2 |
4.下列叙述中正确的是( )
| A. | 在周期表里,主族元素所在的族序数等于原子核外电子数 | |
| B. | 元素周期表有7个主族、7个副族、1个0族、1个Ⅷ族,共18个纵行 | |
| C. | 除短周期外,其他周期均有18种元素 | |
| D. | X2+的核外电子数目为18,则X在第三周期第ⅡA族 |
3.工业制硫酸的一步重要反应是SO2在400~600℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下列有关说法错误的是( )
| A. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| B. | 达到平衡时,SO2的浓度与SO3的浓度相等 | |
| C. | 为了提高SO2的转化率,应适当提高O2的浓度 | |
| D. | 使用催化剂是为了加快反应速率,提高生产效率 |
2.下列关于碱金属的叙述叙述正确的是( )
| A. | 碱金属元素阳离子的氧化性随着原子序数的递增依次增强 | |
| B. | 碱金属的密度随着原子序数的递增逐渐减小 | |
| C. | 随着原子序数的递增,碱金属元素最高价氧化物的水化物的碱性依次减弱 | |
| D. | 钾与氧气或水反应比钠的反应剧烈,铷、铯发生类似的反应更剧烈 |
1.氢氧燃料电池已用于航天飞机,以30%KOH溶液为电解质溶液.电极反应如下:2H2+4OH--4e-=4H2O,O2+2H2O+4e-=4OH-.据此作出判断,下列说法中不正确的是( )
| A. | O2在正极发生还原反应 | B. | 供电时的总反应为2H2+O2═2H2O | ||
| C. | 燃料电池的能量转化率可达100% | D. | 氢氧燃料电池属于环境友好电池 |
20.下列关于化学观或化学研究方法的叙述中错误的是( )
| A. | 增加炼铁高炉的高度可以降低尾气中CO的含量 | |
| B. | 在元素周期表的金属和非金属分界线附近寻找半导体材料 | |
| C. | 控制实验条件可以改变可逆反应的限度和速率 | |
| D. | 在化工生产中应遵循“绿色化学”的思想 |
19.下列各组互为同位素的是( )
| A. | H2O和D2O | B. | ${\;}_{6}^{12}$C和${\;}_{6}^{14}$C | ||
| C. | H2和D2 | D. | O2和O3 |
18.下列物质中既含有离子键,又含有极性共价键的是( )
| A. | NaOH | B. | H2O | C. | MgCl2 | D. | Na2O2 |
17.下列说法中正确的是( )
0 158752 158760 158766 158770 158776 158778 158782 158788 158790 158796 158802 158806 158808 158812 158818 158820 158826 158830 158832 158836 158838 158842 158844 158846 158847 158848 158850 158851 158852 158854 158856 158860 158862 158866 158868 158872 158878 158880 158886 158890 158892 158896 158902 158908 158910 158916 158920 158922 158928 158932 158938 158946 203614
| A. | 吸热反应在不加热的条件下一定不能发生 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 由“100KPa时石墨转化为金刚石,要吸收1.895kJ的热能”可知在100KPa压强下石墨比金刚石稳定 | |
| D. | 化学反应中的能量变化,只表现为热能的变化 |
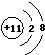 ;D在周期表中位置第三周期第VIA族;E的化学式Na2O2.
;D在周期表中位置第三周期第VIA族;E的化学式Na2O2.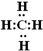 ;
;