6.3月22日是世界水日.下列有关水的说法中不正确的是( )
| A. | 用太阳能蒸馏海水是海水淡化的方法之一 | |
| B. | 推广使用无磷洗衣粉主要是为了防止水体富营养化 | |
| C. | 水厂常用硫酸亚铁和氯气处理水,可起到消毒杀菌和除去水中悬浮杂质的作用 | |
| D. | 水在3.98℃时,主要以(H2O)2存在,这两个水分子间是以共价键相结合的 |
5.在一定条件下的可逆反应中,关于反应速率和达到化学平衡时,下列说法不正确的是( )
| A. | 温度只能改变某一个方向的反应速率 | |
| B. | 决定反应速率的主要因素是反应物的性质 | |
| C. | 反应体系中混合物的组成保持不变 | |
| D. | 正、逆反应速率相等但不为零 |
4.下列过程中,只破坏离子键的是( )
| A. | NO2被木炭吸附 | B. | NaHSO4加热至熔化 | ||
| C. | KHSO4晶体溶于水 | D. | Na2O2溶于水 |
3.下列关于铝及其化合物的说法中不正确的是( )
| A. | 铝既可以用于食品包装,也可以用于建筑材料 | |
| B. | 氧化铝既可以用来冶炼铝,也可用作耐火材料 | |
| C. | 氢氧化铝既可以用于治疗胃酸过多,也可用来制备一些铝盐 | |
| D. | 明矾既能用来净水,也可用作消毒剂 |
2.下列说法正确的是( )
| A. | 氯水和二氧化硫都具有漂白作用,两者漂白原理相同 | |
| B. | 等质量的铜粉按a、b两种途径完全转化,途径a和途径b消耗的H2SO4相等,途径a:Cu$→_{△}^{O_{2}}$CuO$?_{加热}^{稀H_{2}SO_{4}}$CuSO4;途径b:Cu$→_{△}^{浓硫酸}$CuSO4 | |
| C. | 不用其它化学试剂只用适当仪器就可以区别NaCO3溶液和稀硫酸 | |
| D. | 从海水中提取物质都必须通过化学反应才能实现 |
1.某化学实验室产生的废液中含有Fe3+、Cu2+、Zn2+、Cl-四种离子,现设计下列方案对废液进行处理,以回收金属并制备较纯净的氯化锌、氯化铁晶体.
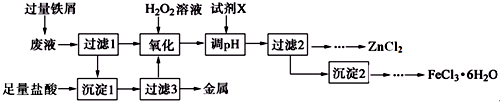
(1)氧化过程中加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O,加入H2O2后立即有大量气泡生成,可能的原因是溶液中金属阳离子催化H2O2分解.
(2)Fe3+水解的平衡常数表达式为Kh=$\frac{{c}^{3}({H}^{+})}{c(F{e}^{3+})}$,加入试剂X调pH合适范围为[3.7,5.4),X可以是下列试剂中的AD(填字母).
A.ZnCO3 B.NH3•H2O C.ZnCl2 D.ZnO
(3)由沉淀2获得FeCl3•6H2O晶体的操作为①加入过量盐酸溶解;②蒸发浓缩、冷却结晶;③过滤、洗涤、干燥.

| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 5.2 | 5.4 |
| 完全沉淀pH | 3.7 | 9.6 | 6.9 | 7.8 |
(2)Fe3+水解的平衡常数表达式为Kh=$\frac{{c}^{3}({H}^{+})}{c(F{e}^{3+})}$,加入试剂X调pH合适范围为[3.7,5.4),X可以是下列试剂中的AD(填字母).
A.ZnCO3 B.NH3•H2O C.ZnCl2 D.ZnO
(3)由沉淀2获得FeCl3•6H2O晶体的操作为①加入过量盐酸溶解;②蒸发浓缩、冷却结晶;③过滤、洗涤、干燥.
20.下列涉及学科观点的有关说法正确的是( )
| A. | 微粒观:二氧化碳是由碳原子和氧原子构成的 | |
| B. | 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和 | |
| C. | 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g | |
| D. | 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异 |
19.实验室常用的制取气体的发生装置如下:

(1)仪器a的名称是试管;搭建B装置时,酒精灯应在固体仪器a之前(选填“前”或“后”)放置.
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(3)在实验室制取二氧化碳的研究中,进行了如下实验:
①上述实验中反应的化学方程式是CaCO3+2HCl→CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
③除盐酸的浓度外,上述实验研究的另一个影响反应因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现酸的浓度越大,产生气体的速度越快.与甲比较,对丁分析正确的是ab.(选填编号)
a.反应更为剧烈 b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大 d.粉末状大理石利用率更高.

(1)仪器a的名称是试管;搭建B装置时,酒精灯应在固体仪器a之前(选填“前”或“后”)放置.
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(3)在实验室制取二氧化碳的研究中,进行了如下实验:
| 实验编号 药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
②若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号).
③除盐酸的浓度外,上述实验研究的另一个影响反应因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现酸的浓度越大,产生气体的速度越快.与甲比较,对丁分析正确的是ab.(选填编号)
a.反应更为剧烈 b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大 d.粉末状大理石利用率更高.
17.下列说法正确的是( )
0 158746 158754 158760 158764 158770 158772 158776 158782 158784 158790 158796 158800 158802 158806 158812 158814 158820 158824 158826 158830 158832 158836 158838 158840 158841 158842 158844 158845 158846 158848 158850 158854 158856 158860 158862 158866 158872 158874 158880 158884 158886 158890 158896 158902 158904 158910 158914 158916 158922 158926 158932 158940 203614
| A. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| B. | 分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有3种 | |
| C. | 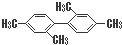 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 | |
| D. | 1mol有机物 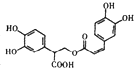 一定条件下能和7molNaOH反应 一定条件下能和7molNaOH反应 |



