16.A、B、C、D、E、F、G、H是元素周期表中八种原子序数依次增大的短周期元素,I是地壳中含量位于第二位的金属元素.已知
①A元素的原子半径在周期表中最小
②B元素原子的最外层电子数是次外层电子数的两倍
③C元素最高价氧化物的水化物和氢化物反应生成盐
④D元素和E元素可形成E2D、E2D2两种离子化合物
⑤H、D两元素同主族,G、H两元素同周期
⑥G元素是同周期中离子半径最小的元素.回答下列问题:
(1)写出B、H两种元素形成化合物的结构式S=C=S,A、D、E三种元素形成的化合物的电子式 ,写出③中生成盐的化学键类型离子键和共价键.
,写出③中生成盐的化学键类型离子键和共价键.
(2)甲、乙、丙分别是B、G、H三种元素最高价含氧酸的钠盐(包括酸式盐),甲、乙都能与丙发生反应,且丙用量不同,反应产物不同.则向甲溶液中缓慢滴加过量的丙溶液,可观察到的实验现象是开始无明显现象,后来生成大量无色气体,向乙溶液中缓慢滴加过量的丙溶液发生的离子反应方程式为H++AlO2-+H2O=Al(OH)3↓和Al(OH)3+3H+=Al3++3H2O.
(3)由元素F和I形成的氢氧化物难溶于水,常温下它们的溶度积如下:
向含有F2+、I3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(F2+):c(I3+)=2.125×1021.
①A元素的原子半径在周期表中最小
②B元素原子的最外层电子数是次外层电子数的两倍
③C元素最高价氧化物的水化物和氢化物反应生成盐
④D元素和E元素可形成E2D、E2D2两种离子化合物
⑤H、D两元素同主族,G、H两元素同周期
⑥G元素是同周期中离子半径最小的元素.回答下列问题:
(1)写出B、H两种元素形成化合物的结构式S=C=S,A、D、E三种元素形成的化合物的电子式
 ,写出③中生成盐的化学键类型离子键和共价键.
,写出③中生成盐的化学键类型离子键和共价键.(2)甲、乙、丙分别是B、G、H三种元素最高价含氧酸的钠盐(包括酸式盐),甲、乙都能与丙发生反应,且丙用量不同,反应产物不同.则向甲溶液中缓慢滴加过量的丙溶液,可观察到的实验现象是开始无明显现象,后来生成大量无色气体,向乙溶液中缓慢滴加过量的丙溶液发生的离子反应方程式为H++AlO2-+H2O=Al(OH)3↓和Al(OH)3+3H+=Al3++3H2O.
(3)由元素F和I形成的氢氧化物难溶于水,常温下它们的溶度积如下:
| 物质 | F(OH)2 | I(OH)3 |
| Ksp | 5.61×10-12 | 2.64×10-39 |
15.四种短周期元素的性质或结构信息如下表.请根据信息回答下列问题.
(1)写出元素T的离子结构示意图 ;写出元素X的气态氢化物的电子式
;写出元素X的气态氢化物的电子式 ;离子半径比较:Y离子>Z离子(填“>”或“<”).
;离子半径比较:Y离子>Z离子(填“>”或“<”).
(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)Z的最高价氧化物对应水化物的电离方程式AlO2-+H2O+H+?Al(OH)3?Al3++3OH-.
(4)元素T与氟元素相比,非金属性较强的是F(用元素符号表示),下列表述中能证明这一事实的是bc
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目.
| 元素 | T | X | Y | Z |
| 性质 结构 信息 | 人体内含量最多的元素,且其单质是常见的助燃剂. | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼. | 单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. | 第三周期元素的简单离子中半径最小 |
 ;写出元素X的气态氢化物的电子式
;写出元素X的气态氢化物的电子式 ;离子半径比较:Y离子>Z离子(填“>”或“<”).
;离子半径比较:Y离子>Z离子(填“>”或“<”).(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)Z的最高价氧化物对应水化物的电离方程式AlO2-+H2O+H+?Al(OH)3?Al3++3OH-.
(4)元素T与氟元素相比,非金属性较强的是F(用元素符号表示),下列表述中能证明这一事实的是bc
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目.
14.下列做法错误的是( )
| A. | 用加热煮沸的方法将硬水软化 | |
| B. | 图书、档案、贵重设备等失火时可以用二氧化碳灭火器灭火 | |
| C. | 包装食品使用的聚氯乙烯塑料袋,可以用加热的方法封口 | |
| D. | 炉具清洁剂中含有氢氧化钠能与油脂发生反应,可以用于去除油污 |
12.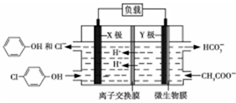 测得某工业废水中含有乙酸钠及对氯酚(
测得某工业废水中含有乙酸钠及对氯酚(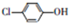 ),为改善水质现利用微生物电池加以去除,反应原理如图所示,下列说法正确的是( )
),为改善水质现利用微生物电池加以去除,反应原理如图所示,下列说法正确的是( )
 测得某工业废水中含有乙酸钠及对氯酚(
测得某工业废水中含有乙酸钠及对氯酚( ),为改善水质现利用微生物电池加以去除,反应原理如图所示,下列说法正确的是( )
),为改善水质现利用微生物电池加以去除,反应原理如图所示,下列说法正确的是( )| A. | X极为微生物电池的负极 | |
| B. | 该电池能够在高温下工作 | |
| C. | 图中离子交换膜应为阴离子交换膜 | |
| D. | Y极电极反应式为:CH3COO--8e-+4H2O═2HCO3-+9H+ |
11.下列各组物质的燃烧热相等的是( )
| A. | 碳和一氧化碳 | B. | 1mol 碳和2mol 碳 | ||
| C. | 1mol 乙炔和2mol 碳 | D. | 淀粉和纤维素 |
8.下列有关实验的说法正确的是( )
| A. | 若用标准盐酸滴定待测 NaOH 溶液,滴定前仰视,滴定后俯视则测定值偏大 | |
| B. | 可用 pH 试纸测定新制氯水的 pH | |
| C. | 中和滴定实验中,洗净后的锥形瓶不需要干燥 | |
| D. | 向白色 ZnS 沉淀上滴加 CuSO4溶液,沉淀变为黑色,说明 Ksp(ZnS)<Ksp(CuS) |
7.氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120o,它能水解,有关叙述正确的是( )
0 158743 158751 158757 158761 158767 158769 158773 158779 158781 158787 158793 158797 158799 158803 158809 158811 158817 158821 158823 158827 158829 158833 158835 158837 158838 158839 158841 158842 158843 158845 158847 158851 158853 158857 158859 158863 158869 158871 158877 158881 158883 158887 158893 158899 158901 158907 158911 158913 158919 158923 158929 158937 203614
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 硼原子以sp杂化 | |
| C. | 氯化硼晶体为分子晶体 | |
| D. | 氯化硼是极性分子 |
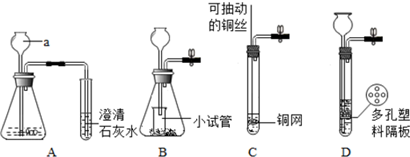

 或
或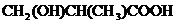 或
或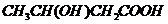 或
或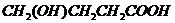


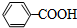
 .
. 研究碳及其化合物的利用对促进低碳社会的构建具有重要的意义.某学习小组查阅资料并进行相关探究,请帮忙完成以下探究.
研究碳及其化合物的利用对促进低碳社会的构建具有重要的意义.某学习小组查阅资料并进行相关探究,请帮忙完成以下探究.