16.强酸和强碱的稀溶液反应的中和热可以表示为:H+(aq)+OH-(aq)=H2O ( l )△H=-57.3kJ•mol-1,
已知:CH3COOH (aq)+NaOH (aq)=CH3COONa (aq)+H2O ( l )△H=-Q1 kJ•mol-1,
$\frac{1}{2}$H2SO4(浓)+NaOH (aq)=$\frac{1}{2}$Na2SO4 (aq)+H2O ( l )△H=-Q2 kJ•mol-1,
上述反应均在溶液中进行,则下列关系正确的是( )
已知:CH3COOH (aq)+NaOH (aq)=CH3COONa (aq)+H2O ( l )△H=-Q1 kJ•mol-1,
$\frac{1}{2}$H2SO4(浓)+NaOH (aq)=$\frac{1}{2}$Na2SO4 (aq)+H2O ( l )△H=-Q2 kJ•mol-1,
上述反应均在溶液中进行,则下列关系正确的是( )
| A. | Q2>Q1>57.3 | B. | Q1=57.3<Q2 | C. | Q2>57.3>Q1 | D. | Q2=57.3>Q1 |
15.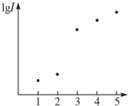 电离能是指从气态原子在基态时失去电子成为阳离子所吸收的能量,如图表示元素X的前五级电离能的对数值,试推测X可能是哪些元素( )
电离能是指从气态原子在基态时失去电子成为阳离子所吸收的能量,如图表示元素X的前五级电离能的对数值,试推测X可能是哪些元素( )
 电离能是指从气态原子在基态时失去电子成为阳离子所吸收的能量,如图表示元素X的前五级电离能的对数值,试推测X可能是哪些元素( )
电离能是指从气态原子在基态时失去电子成为阳离子所吸收的能量,如图表示元素X的前五级电离能的对数值,试推测X可能是哪些元素( )| A. | 第ⅠA族 | B. | 第ⅡA族 | C. | 第ⅢA族 | D. | 第ⅣA族 |
14.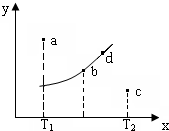 图中的曲线是反应2A(g)+B(g)?2C(g)△H=QkJ/mol在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c、d四点,则下列描述正确的是( )
图中的曲线是反应2A(g)+B(g)?2C(g)△H=QkJ/mol在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c、d四点,则下列描述正确的是( )
 图中的曲线是反应2A(g)+B(g)?2C(g)△H=QkJ/mol在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c、d四点,则下列描述正确的是( )
图中的曲线是反应2A(g)+B(g)?2C(g)△H=QkJ/mol在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c、d四点,则下列描述正确的是( )| A. | Q<0 | |
| B. | 平衡常数值:b点<d点 | |
| C. | T1温度下若由a点达到平衡,可以采取增大压强的方法 | |
| D. | c点v(正)<v(逆) |
12.设NO+NO2?NO2+CO(正反应吸热)反应速率为v1;N2+3H2?NH3(正反应放热)反应速率为v2.对于前述反应,当温度升高时,v1和v2变化情况为( )
| A. | v1增大,v2减小 | B. | v1减小,v2增大 | C. | 同时增大 | D. | 同时减小 |
10.火法炼铜的原理为Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2,下列说法中正确的是( )
| A. | Cu2S只作还原剂 | |
| B. | 该反应是氧化还原反应 | |
| C. | S元素被还原 | |
| D. | 当1 mol O2参加反应时,共转移4 mol e- |
9.在N2 (g)+3H2(g)?2NH3 (g)的平衡体系中,其他条件不变,增加氮气的浓度,下列判断正确的是( )
| A. | 氮气的转化率减小 | |
| B. | 氢气的转化率增大 | |
| C. | 氨气在平衡混合气体中的百分含量一定增大 | |
| D. | 氨气的分解速率大于氨气的生成速率 |
8.在2L的密闭容器中,一定量的A和B发生反应:3A(g)+B(g)?xC(g)+2D(g),经测定5min内C的平均反应速率是0.1mol/(L•min),同时生成1mol D.下列有关说法正确的是( )
| A. | 5min内D的平均反应速率是0.2mol/(L•min) | |
| B. | 3υA=2υD | |
| C. | x的值是2 | |
| D. | A的起始物质的量为1.5mol |
7.化学与环境密切相关.下列措施不利于“蓝天工程”建设的是( )
0 158741 158749 158755 158759 158765 158767 158771 158777 158779 158785 158791 158795 158797 158801 158807 158809 158815 158819 158821 158825 158827 158831 158833 158835 158836 158837 158839 158840 158841 158843 158845 158849 158851 158855 158857 158861 158867 158869 158875 158879 158881 158885 158891 158897 158899 158905 158909 158911 158917 158921 158927 158935 203614
| A. | 开发利用太阳能、风能等,减少对化石能源的依赖 | |
| B. | 监测大气中的PM2.5,改善空气质量 | |
| C. | 大力实施矿物燃料和脱硫脱硝技术以减少SO2、NOx的排放 | |
| D. | 加高工厂烟囱,使烟尘和废气远离地表 |
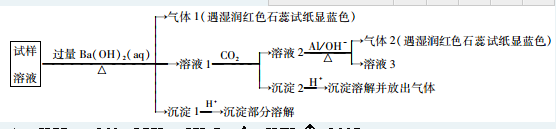

 .
.