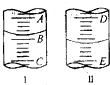
17.关于如图装置的说法正确的是( )
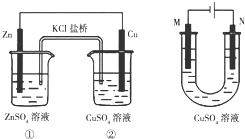

| A. | 装置①将电能转变为化学能 | |
| B. | 装置①中盐桥内的Cl-移向ZnSO4溶液 | |
| C. | 若装置②用于铁棒镀铜,则N极为铁棒 | |
| D. | 若装置②用于电解精炼铜,则溶液中的Cu2+浓度保持不变 |
16.下列实验可达到实验目的是( )
| A. | 可加入酸性KMnO4溶液鉴别苯、环己烯和己烷 | |
| B. | 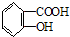 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 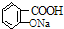 | |
| C. | 向卤代烃水解后的溶液中直接加入硝酸银溶液,可以确定卤代烃中的卤元素 | |
| D. | 利用盐析、过滤可将蛋白质和NaCl溶液分离 |
15.下列溶液中能大量共存的离子组是( )
| A. | 加入铝粉能产生H2的溶液:Fe2+、NH4+、SO42-、NO3- | |
| B. | 室温下水电离出c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- | |
| C. | 含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl- | |
| D. | 使PH试纸呈深蓝色的溶液:Na+、K+、AlO2-、CO32- |
14.设NA为阿伏加德罗常数的值.下列叙述不正确的是( )
| A. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.25NA | |
| B. | 常温常压下,6.4 g氧气和臭氧的混合气体中含有的原子总数为0.4NA | |
| C. | 惰性电极电解饱和食盐水,若电路中通过NA个电子,则阳极产生气体11.2L | |
| D. | 常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
13.二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
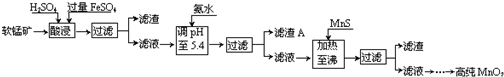
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
(1)FeSO4在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为2FeSO4+MnO2+2H2SO4=MnSO4+Fe2(SO4)3+2H2O.
(2)pH要调到5.4,应该使用pH计或精密pH试纸(填写仪器或试剂名称)来测量.滤渣A的主要成分是Fe(OH)3和Al(OH)3.
(3)碱性锌锰电池中,MnO2参与的电极反应方程式为MnO2+H2O+e-=MnOOH+OH-.
(4)MnO2可作超级电容器材料.用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是Mn2++2H2O-2e-═MnO2+4H+.
(5)已知25℃时,Ksp[Fe(OH)3]=2•79×10-58,该温度下反应Fe(OH)3+3H+═Fe3++3H2O的平衡常数K=2.79×103.

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)pH要调到5.4,应该使用pH计或精密pH试纸(填写仪器或试剂名称)来测量.滤渣A的主要成分是Fe(OH)3和Al(OH)3.
(3)碱性锌锰电池中,MnO2参与的电极反应方程式为MnO2+H2O+e-=MnOOH+OH-.
(4)MnO2可作超级电容器材料.用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是Mn2++2H2O-2e-═MnO2+4H+.
(5)已知25℃时,Ksp[Fe(OH)3]=2•79×10-58,该温度下反应Fe(OH)3+3H+═Fe3++3H2O的平衡常数K=2.79×103.
11.下列关于实验操作的叙述正确的是( )
| A. | 石蕊试纸和pH试纸使用前都必须用蒸馏水润湿 | |
| B. | 向沸水中滴加饱和氯化铁溶液并不断搅拌,制取氢氧化铁胶体 | |
| C. | 中和滴定实验时,滴定前仰视刻度,滴定后俯视,则对测得浓度无影响 | |
| D. | 滴定管盛装滴定液前需先用蒸馏水洗净,再用滴定液润洗 |
10.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法错误的是( )


| A. | 该反应的热化学方程式为:N2(g)+O2(g)=2NO(g)△H=+180 kJ•mol-1 | |
| B. | 1 mol N2(l)和NA个 O2(l)反应生成2mol NO(g)时,吸收的能量为180 kJ | |
| C. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| D. | 通常情况下,N2(g)和O2(g)混合不能直接生成NO(g) |
9.pH=3和 PH=5的盐酸,等体积混合,混合后(假设体积不变)的PH为( )
| A. | 3 | B. | 3.1 | C. | 3.2 | D. | 3.3 |
8.5个碳的烷烃的同分异构体共有( )
0 158734 158742 158748 158752 158758 158760 158764 158770 158772 158778 158784 158788 158790 158794 158800 158802 158808 158812 158814 158818 158820 158824 158826 158828 158829 158830 158832 158833 158834 158836 158838 158842 158844 158848 158850 158854 158860 158862 158868 158872 158874 158878 158884 158890 158892 158898 158902 158904 158910 158914 158920 158928 203614
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
 草酸晶体的组成可用H2C2O4•xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100mL水溶液.量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol•L-1的KMnO4溶液滴定,所发生的反应:KMnO4+H2C2O4+H2SO4=K2SO4+CO2↑+MnSO4+H2O
草酸晶体的组成可用H2C2O4•xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100mL水溶液.量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol•L-1的KMnO4溶液滴定,所发生的反应:KMnO4+H2C2O4+H2SO4=K2SO4+CO2↑+MnSO4+H2O