14.25℃时,将amol•L-1、pH=m的一元酸HX溶液与bmol•L-1、pH=n的一元碱YOH溶液等体积混合,下列说法正确的是( )
| A. | 若a=b,则混合后溶液中一定有:c(X-)=c(Y+)>c(H+)=c(OH-) | |
| B. | 若m+n=14,则混合后溶液一定显中性 | |
| C. | 若混合后溶液中c(X-)<c(Y+),则该混合溶液一定显碱性 | |
| D. | 若a=b,混合后溶液pH<7,则一定生成强酸弱碱盐 |
13.已知酸性强弱顺序为H2CO3>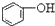 >HCO3-,下列化学方程式正确的是( )
>HCO3-,下列化学方程式正确的是( )
 >HCO3-,下列化学方程式正确的是( )
>HCO3-,下列化学方程式正确的是( )| A. | 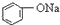 +H2O+CO2→ +H2O+CO2→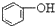 +Na2CO3 +Na2CO3 | B. | 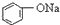 +NaHCO3→ +NaHCO3→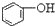 +Na2CO3 +Na2CO3 | ||
| C. | 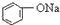 +H2O+CO2→ +H2O+CO2→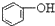 +NaHCO3 +NaHCO3 | D. | 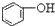 +NaHCO3→ +NaHCO3→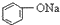 +H2O+CO2 +H2O+CO2 |
12.下列各物质中互为同系物的是( )
| A. | 苯、溴苯 | B. | 正丁烷和异丁烷 | C. |  和 和 | D. |  和 和 |
10.下列关于苯的叙述正确的是( )
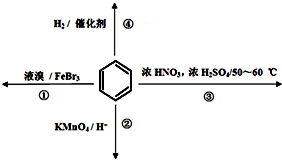

| A. | 反应①常温下不能进行 | |
| B. | 反应②不发生,但是仍有分层现象,紫色层在下层 | |
| C. | 反应③为加成反应 | |
| D. | 反应④能发生,从而证明苯中是单双键交替结构 |
9.16O与18O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是( )
0 158726 158734 158740 158744 158750 158752 158756 158762 158764 158770 158776 158780 158782 158786 158792 158794 158800 158804 158806 158810 158812 158816 158818 158820 158821 158822 158824 158825 158826 158828 158830 158834 158836 158840 158842 158846 158852 158854 158860 158864 158866 158870 158876 158882 158884 158890 158894 158896 158902 158906 158912 158920 203614
| A. | 16O2与18O2互为同位素 | |
| B. | 16O与18O核外电子排布方式不同 | |
| C. | 通过化学变化可以实现16O2与18O2间的相互转化 | |
| D. | 标准状况下,1.12L16O2和1.12L18O2均含0.1NA个氧原子 |
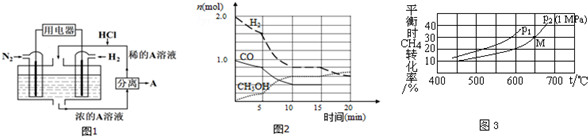
 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O. ,它是一种稠环芳香烃,其化学式为C20H12,此物质中碳元素和氢元素的质量比为20:1.
,它是一种稠环芳香烃,其化学式为C20H12,此物质中碳元素和氢元素的质量比为20:1.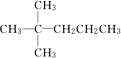 .
. 、
、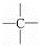 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如:
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如: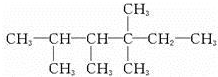


 .
.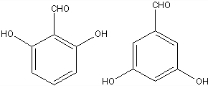 、
、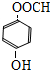 (任意一种).
(任意一种).