3.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下22.4L甲醇中含共价键数为5NA | |
| B. | 500ml 1mol/L醋酸溶液中含氧原子数为NA | |
| C. | 28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| D. | 1 mol的羟基与1 moL的氢氧根离子所含电子数均为9 NA |
2.去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示.下列说法不正确的是( )
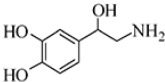

| A. | 每个去甲肾上腺素分子中含有2个酚羟基 | |
| B. | 去甲肾上腺素能与酸性KMnO4溶液反应 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
1.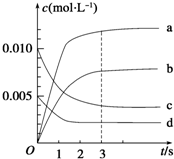 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:
(1)能说明该反应已经达到平衡状态的是bc
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(2)图中表示NO2的变化的曲线是b,
(3)用O2的浓度变化表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是ac
a.将容器体积变为1Lb.适当升高温度c.增大O2的浓度d.选择高效的催化剂.
 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(2)图中表示NO2的变化的曲线是b,
(3)用O2的浓度变化表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是ac
a.将容器体积变为1Lb.适当升高温度c.增大O2的浓度d.选择高效的催化剂.
18.下列叙述不正确的是( )
0 158725 158733 158739 158743 158749 158751 158755 158761 158763 158769 158775 158779 158781 158785 158791 158793 158799 158803 158805 158809 158811 158815 158817 158819 158820 158821 158823 158824 158825 158827 158829 158833 158835 158839 158841 158845 158851 158853 158859 158863 158865 158869 158875 158881 158883 158889 158893 158895 158901 158905 158911 158919 203614
| A. | 铁制品表面镀锌可以增强其抗腐蚀性 | |
| B. | 在海轮外壳上连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| C. | 马口铁(镀锡)外层镀层被破坏后,里面的铁更易被腐蚀 | |
| D. | 利用外加电流的阴极保护法,可以将水下的钢闸门与电源正极相连 |
 “摩尔盐”1(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂.已知:摩尔盐隔绝空气加热至500℃时可完全分解.某学习小组欲探究其分解产物.
“摩尔盐”1(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂.已知:摩尔盐隔绝空气加热至500℃时可完全分解.某学习小组欲探究其分解产物.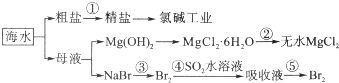
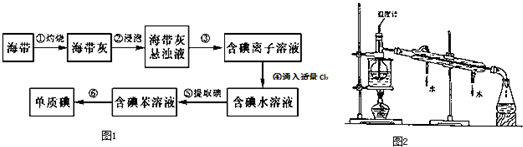
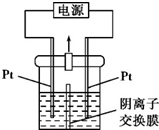 某实验小组的同学用图所示的实验装置进行电解反应,电解槽内装有KI-淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.
某实验小组的同学用图所示的实验装置进行电解反应,电解槽内装有KI-淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.