7.实验室欲配制100mL 0.5mol/L的NaOH溶液,配制过程中的下列做法会使所配浓度偏高的是( )
| A. | 称量NaOH固体时,放在烧杯中且称量较慢 | |
| B. | 定容时,俯视刻度线 | |
| C. | 定容时,加水超过刻度线,再用胶头滴及将过线的液体吸出 | |
| D. | 移液前,容量瓶中有少量蒸馏水 |
19.位于前四周期的6种主族元素A、B、C、D、E、F原子序数依次增大,其中B、D同主族,D、E同周期.A、B、C在周期表中相邻,且三种元素的原子最外层电子数之和为18.F是其所在周期中最活泼的金属元素.根据推断回答下列问题:
(1)A在周期表中的位置第二周期、ⅤA族:写出D与F形成的最简单离子化合物的电子式K+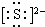 K+.
K+.
(2)用“>”或“<”填空:
(3)一定条件,在水溶液中1mol E-、EBx-(x=1,2,3,4)的能量(KJ)相对大小如图所示.
①d点对应的微粒是ClO4-(填离子符号)
②b→a+c反应的离子方程式为3ClO-=ClO3-+2Cl-,该反应是放热反应(填“吸热”或“放热”)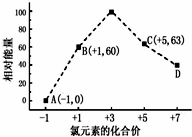
0 158721 158729 158735 158739 158745 158747 158751 158757 158759 158765 158771 158775 158777 158781 158787 158789 158795 158799 158801 158805 158807 158811 158813 158815 158816 158817 158819 158820 158821 158823 158825 158829 158831 158835 158837 158841 158847 158849 158855 158859 158861 158865 158871 158877 158879 158885 158889 158891 158897 158901 158907 158915 203614
(1)A在周期表中的位置第二周期、ⅤA族:写出D与F形成的最简单离子化合物的电子式K+
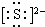 K+.
K+.(2)用“>”或“<”填空:
| 离子半径 | 非金属性 | 酸性 | 沸点 |
| F+<D2- | A<B | D的最高价氧化物的水化物<E的最高价氧化物的水化物 | C的氢化物>E的氢化物 |
①d点对应的微粒是ClO4-(填离子符号)
②b→a+c反应的离子方程式为3ClO-=ClO3-+2Cl-,该反应是放热反应(填“吸热”或“放热”)


 .
. 等.
等.
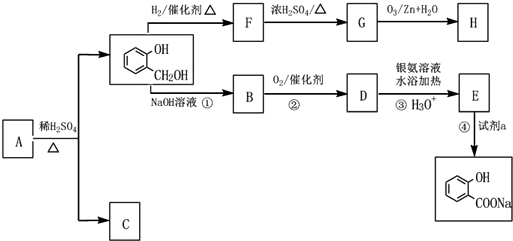
 为原料制备化合物X(结构简式见图
为原料制备化合物X(结构简式见图 )
) ;该元素最高正化合价与最低负化合价分别是+6和-2.
;该元素最高正化合价与最低负化合价分别是+6和-2.
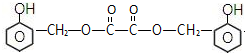 ,C俗称为草酸;
,C俗称为草酸; ; 写出C与对苯二甲醇在一定条件下发生缩聚反应的化学反应方程式:
; 写出C与对苯二甲醇在一定条件下发生缩聚反应的化学反应方程式: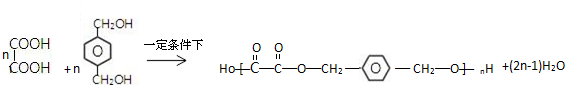 ;
; ;
;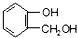 不能发生缩聚反应
不能发生缩聚反应 到F反应是否进行完全,可用FeCl3溶液检验
到F反应是否进行完全,可用FeCl3溶液检验 ;
;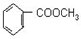 的最佳路线流程图(不参考答案能选用其他任何有机试剂,无机试剂任选). 流程图示例如下:
的最佳路线流程图(不参考答案能选用其他任何有机试剂,无机试剂任选). 流程图示例如下:
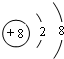 ;
;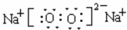 ;
;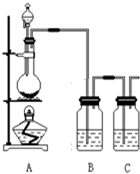 为了验证氯元素的非金属性比碘元素的非金属性强,某化学实验小组利用题中所给试剂设计了如下实验,请回答下列问题:
为了验证氯元素的非金属性比碘元素的非金属性强,某化学实验小组利用题中所给试剂设计了如下实验,请回答下列问题: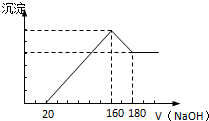 将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为2mol/L的NaOH溶液,生成的沉淀与加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为2mol/L的NaOH溶液,生成的沉淀与加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)