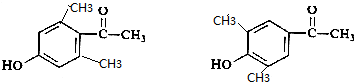3.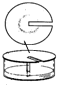 常温下,在丙酮-盐酸混合溶液中,Fe3+比Cu2+的溶解度更大,用该溶液作展开剂分离Fe3+和Cu2+的装置如图.以下叙述错误的是( )
常温下,在丙酮-盐酸混合溶液中,Fe3+比Cu2+的溶解度更大,用该溶液作展开剂分离Fe3+和Cu2+的装置如图.以下叙述错误的是( )
 常温下,在丙酮-盐酸混合溶液中,Fe3+比Cu2+的溶解度更大,用该溶液作展开剂分离Fe3+和Cu2+的装置如图.以下叙述错误的是( )
常温下,在丙酮-盐酸混合溶液中,Fe3+比Cu2+的溶解度更大,用该溶液作展开剂分离Fe3+和Cu2+的装置如图.以下叙述错误的是( )| A. | 该方法为径向纸上层析法 | B. | 试样点需浸没于展开剂中 | ||
| C. | 试样点晾干或电风吹干后才能补滴 | D. | 喷浓氨水内层圆环色斑呈绛蓝色 |
2.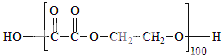 无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在未来科技发展中发挥着重要的作用.
无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在未来科技发展中发挥着重要的作用.
(1)新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等.将5.60g α-Fe粉与一定量水蒸气在高温下反应一定时间后冷却,其质量变为6.88g.
①产生的氢气的体积为1792mL(标准状况下).
②将冷却后的固体物质放入足量FeCl3溶液中充分反应(已知Fe3O4不溶于FeCl3溶液),计算最多消耗FeCl3的物质的量.
(2)Nierite是一种高熔点高硬度的陶瓷材料.Nierite的摩尔质量为140g/mol,其中硅元素的质量分数为60%.已知1mol NH3与足量的化合物T充分反应后可得到35g Nierite与3mol HCl气体.Nierite的化学式为Si3N4.T的化学式为SiCl4.
(3))K金是常见的贵金属材料,除黄金外,还含有银、铜中的一种或两种金属.为测定某18K金样品的组成,将2.832g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224mL(折算至标准状况,下同),将该混合气体与84mL O2混合后缓缓通入水中,恰好被完全吸收.
①混合气体的平均摩尔质量为69g/mol.
②填写该18K金的成分表(精确至0.01%,若不含该金属则填0).
(4)有机高分子材料聚酯纤维可由二酸与二醇通过缩聚形成.如100个乙二酸分子与100个乙二醇分子发生缩聚,当形成一条聚酯链时,其(平均)式量达到最大(如图所示,其式量为11618).
为降低聚酯链的长度与平均式量,可调整乙二酸与乙二醇的相对用量,使形成的聚酯链两端均为相同基团,从而无法再连接增长.现有100个乙二酸分子与105个乙二醇分子恰好完全反应,且聚酯链无法再增长.
①共形成5条聚酯链.
②计算所得聚酯的平均式量.
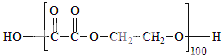 无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在未来科技发展中发挥着重要的作用.
无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,在未来科技发展中发挥着重要的作用.(1)新型材料α-Fe粉具有超强的磁性能,用作高密度磁记录的介质以及高效催化剂等.将5.60g α-Fe粉与一定量水蒸气在高温下反应一定时间后冷却,其质量变为6.88g.
①产生的氢气的体积为1792mL(标准状况下).
②将冷却后的固体物质放入足量FeCl3溶液中充分反应(已知Fe3O4不溶于FeCl3溶液),计算最多消耗FeCl3的物质的量.
(2)Nierite是一种高熔点高硬度的陶瓷材料.Nierite的摩尔质量为140g/mol,其中硅元素的质量分数为60%.已知1mol NH3与足量的化合物T充分反应后可得到35g Nierite与3mol HCl气体.Nierite的化学式为Si3N4.T的化学式为SiCl4.
(3))K金是常见的贵金属材料,除黄金外,还含有银、铜中的一种或两种金属.为测定某18K金样品的组成,将2.832g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224mL(折算至标准状况,下同),将该混合气体与84mL O2混合后缓缓通入水中,恰好被完全吸收.
①混合气体的平均摩尔质量为69g/mol.
②填写该18K金的成分表(精确至0.01%,若不含该金属则填0).
| 18K金成分 | Au | Ag | Cu |
| 含量(质量分数) | 75.00% | 11.44% | 13.56% |
为降低聚酯链的长度与平均式量,可调整乙二酸与乙二醇的相对用量,使形成的聚酯链两端均为相同基团,从而无法再连接增长.现有100个乙二酸分子与105个乙二醇分子恰好完全反应,且聚酯链无法再增长.
①共形成5条聚酯链.
②计算所得聚酯的平均式量.
20.在探究氯水成分的实验中,下列根据实验现象得出的结论错误的是( )
| 实验序号 | 实验现象 | 实验结论 |
| A | 氯水呈浅黄绿色 | 氯水中含有Cl2 |
| B | 向FeCl2溶液中滴加氯水,溶液变成棕黄色 | 氯水中含有HClO |
| C | 向氯水中滴加硝酸酸化的 AgNO3溶液,产生白色沉淀 | 氯水中含有Cl- |
| D | 向氯水中加入NaHCO3粉末,有气泡产生 | 氯水中含有H+ |
| A. | A | B. | B | C. | C | D. | D |
19.温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)═PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据见表:
下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50s 的平均速率 (PCl3)=0.0032mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时 (PCl3)=0.11mol•L-1,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2,反应达到平衡前 (正)>(逆) | |
| D. | 相同温度下,起始时向容器中充入2.0mol PCl3和2.0mol Cl2,达到平衡时,PCl3的转化率小于80% |
18.下列说法正确的是( )
| A. | 糖类在一定条件下可以水解生成乙醇和二氧化碳 | |
| B. | 检验淀粉在稀硫酸催化条件下水解产物的方法:取适量水解液于试管中,加入少量新制Cu(OH)2溶液,加热,观察是否出现砖红色沉淀 | |
| C. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 | |
| D. | 蛋白质在紫外线、CuSO4溶液、福尔马林作用下均会发生变性 |
15.下列物质与水反应,能放出氧气的是( )
0 158715 158723 158729 158733 158739 158741 158745 158751 158753 158759 158765 158769 158771 158775 158781 158783 158789 158793 158795 158799 158801 158805 158807 158809 158810 158811 158813 158814 158815 158817 158819 158823 158825 158829 158831 158835 158841 158843 158849 158853 158855 158859 158865 158871 158873 158879 158883 158885 158891 158895 158901 158909 203614
| A. | Na | B. | Na2O | C. | Na2O2 | D. | Al |
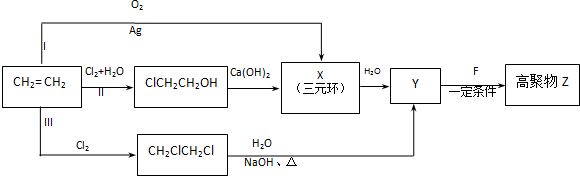
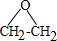 .
.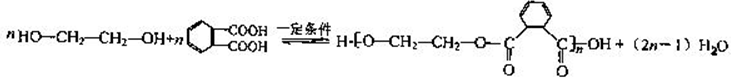 CH2ClCH2Cl→Y:CH2ClCH2Cl+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaCl.
CH2ClCH2Cl→Y:CH2ClCH2Cl+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaCl.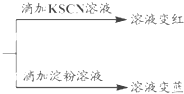
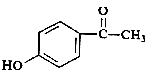 写出同时符合下列条件的同分异构体:
写出同时符合下列条件的同分异构体: