3.已知:a H2S(g)+b O2(g)═c X+d H2O(1)△H.当X为下列何种物质(状态)时,该反应热(△H)最小( )
| A. | S(s) | B. | S(g) | C. | SO2(l) | D. | SO2(g) |
2.能够大量共存的离子组合是( )
| A. | H+、SO42-、NO3-、Ba2+ | B. | K+、Cl-、CO32-、Na+ | ||
| C. | Cu2+、NO3-、OH-、Na+ | D. | K+、SO42-、HCO3-、H+ |
1.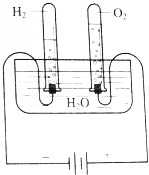 (1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?
(1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?
(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成O2、H2的质量,根据O2、H2的摩尔质量,计算物质的量,并通过下表进行比较.
根据该实验的观察与推算能否初步得出下列结论:在相同温度和压强下.1molO2和H2的体积相同.
 (1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?
(1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成O2、H2的质量,根据O2、H2的摩尔质量,计算物质的量,并通过下表进行比较.
| 质量g | 物质的量 | H2 和O2物质的量的比 | |
| H2 | |||
| O2 |
20.在盛有硫酸铜饱和溶液的恒温密闭容器中,投入一块形状不规则的硫酸铜晶体,放置数天后,发生的变化是( )
| A. | 晶体形状改变且质量减少 | |
| B. | 晶体形状改变而质量不变 | |
| C. | 晶体形状和质量都不变 | |
| D. | 硫酸铜溶液的物质的量浓度有所增大 |
19.关于下列装置用途的判断正确的是( )
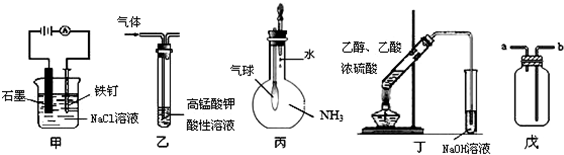
①装置甲可防止铁钉被腐蚀
②装置乙可除去甲醛中混有的乙烯
③装置丙可检验 NH3气体在水中的溶解性④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集 H2、CO2、Cl2、HCl、NO2等气体.

①装置甲可防止铁钉被腐蚀
②装置乙可除去甲醛中混有的乙烯
③装置丙可检验 NH3气体在水中的溶解性④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集 H2、CO2、Cl2、HCl、NO2等气体.
| A. | 只有③④ | B. | 只有③⑤ | C. | 只有①③⑤ | D. | 只有①②④ |
18.下列方案能够达到实验目的是( )
| A. | 用浓溴水除去苯中的苯酚 | |
| B. | 除去苯中的少量甲苯,先用酸性高锰酸钾溶液,后用氢氧化钠溶液处理 | |
| C. | 在加热条件下,用乙醇除去乙酸乙酯中的乙酸 | |
| D. | 将溴乙烷和氢氧化钠溶液混合加热后,再加入硝酸银溶液,检验溴元素 |
17.根据元素周期表和元素周期律分析下面的推断,其中不正确的是( )
| A. | 氢氧化钡比氢氧化钙的碱性强 | |
| B. | HBrO4的酸性比HIO4强 | |
| C. | 铍(Be)原子失电子的能力比镁弱 | |
| D. | 硒(Se)化氢的稳定性比硫化氢的稳定性强 |
16.用2mol/L的硝酸银溶液10mL,分别与相同体积的下列溶液恰好完全反应,则下列溶液中物质的量浓度最小的是( )
| A. | BaCl2 | B. | MgCl2 | C. | KCl | D. | FeCl3 |
15.设NA表示阿伏加德罗常数,下列叙述正确的是( )
0 158713 158721 158727 158731 158737 158739 158743 158749 158751 158757 158763 158767 158769 158773 158779 158781 158787 158791 158793 158797 158799 158803 158805 158807 158808 158809 158811 158812 158813 158815 158817 158821 158823 158827 158829 158833 158839 158841 158847 158851 158853 158857 158863 158869 158871 158877 158881 158883 158889 158893 158899 158907 203614
| A. | 1.7g OH- 所含电子数为0.9NA | |
| B. | 标准状况下,11.2 L HCl 所含质子数为18NA | |
| C. | 常温下,11.2 L Cl2 气所含原子数为NA | |
| D. | 0.5 mol D2O 中所含质子数为5NA |