14.已知有下列反应:4KI+2CuSO4=I2+Cu2I2↓(白色)+2K2SO4;I2+2S2O32-═S4O62-+2I-;Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O
(1)现要测定100.00mL硫酸铜溶液中铜离子的物质的量浓度,其测定过程如下:用移液管准确量取20,.00mL硫酸铜溶液于锥形瓶中,加入过量KI固体,充分反应,生成白色沉淀,用0,.1000mol/LNa2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液19.80mL.
①滴定过程应选用作指示剂淀粉,滴定终点的现象是最后一滴溶液滴下,溶液恰好由蓝色变为无色,且半分钟内不变化.
②下列有关该实验中的图示和操作都正确的是C.
A.图A表示用移液管移取A溶液到锥形瓶中的操作 B.图B表示对滴定管读数
C.图C表示排气泡操作 D.图D表示滴定操作

③溶液A中铜离子的物质的量浓度为0.099mol/L.
④下列实验操作会使得测定结果偏高的是B.
A.锥形瓶用蒸馏水洗涤后,直接盛待测液
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴无气泡
C.摇荡锥形瓶时溶液溅出
D.锥形瓶中溶液颜色发生变化时立即读数
(2)某实验兴趣小组为了研究外界条件对Na2S2O3与硫酸反应速率的影响,设计如下实验方案:
①判断上述反应速率快慢的实验现象是出现淡黄色沉淀的快慢.
②实验比较法是人们研究各类问题常用的方法,但在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰.上述A组和B组比较的是硫酸浓度的改变对反应速率的影响,则B组中加水的体积a=10mL.
③由A组和C组实验比较可以得出的结论是其他条件相同时,温度越高,反应速率越快.
(1)现要测定100.00mL硫酸铜溶液中铜离子的物质的量浓度,其测定过程如下:用移液管准确量取20,.00mL硫酸铜溶液于锥形瓶中,加入过量KI固体,充分反应,生成白色沉淀,用0,.1000mol/LNa2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液19.80mL.
①滴定过程应选用作指示剂淀粉,滴定终点的现象是最后一滴溶液滴下,溶液恰好由蓝色变为无色,且半分钟内不变化.
②下列有关该实验中的图示和操作都正确的是C.
A.图A表示用移液管移取A溶液到锥形瓶中的操作 B.图B表示对滴定管读数
C.图C表示排气泡操作 D.图D表示滴定操作

③溶液A中铜离子的物质的量浓度为0.099mol/L.
④下列实验操作会使得测定结果偏高的是B.
A.锥形瓶用蒸馏水洗涤后,直接盛待测液
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴无气泡
C.摇荡锥形瓶时溶液溅出
D.锥形瓶中溶液颜色发生变化时立即读数
(2)某实验兴趣小组为了研究外界条件对Na2S2O3与硫酸反应速率的影响,设计如下实验方案:
组号 | 反应温度 (℃) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/ml | c/mol•L-1 | V/ml | c/mol•L-1 | V/ml | ||
| A | 10 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | a |
| C | 30 | 5 | 0.1 | 10 | 0.1 | 5 |
②实验比较法是人们研究各类问题常用的方法,但在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰.上述A组和B组比较的是硫酸浓度的改变对反应速率的影响,则B组中加水的体积a=10mL.
③由A组和C组实验比较可以得出的结论是其他条件相同时,温度越高,反应速率越快.
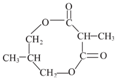
13.某有机物结构简式为: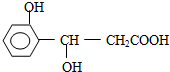 ,它不可能发生的反应类型( )
,它不可能发生的反应类型( )
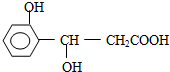 ,它不可能发生的反应类型( )
,它不可能发生的反应类型( )| A. | 取代 | B. | 氧化 | C. | 水解 | D. | 酯化 |
12.铁元素及其化合物与人类的生产生活息息相关,回答下列问题
(1)铁酸钠(Na 2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe 3+.
①铁酸钠中铁元素的化合价为+6.
②铁酸钠用于水处理,除了能消毒杀菌外,还可以像明矾【KAl(SO4)2】一样起到净水作用,请说明明矾的净水原理:Al3++3H2O?Al(OH)3+3H+.(用离子方程式表示)
(2)反应ⅠFe(s)+CO 2 (g)?FeO(s)+CO(g)△H=a kJ?mol -1,平衡常数为K;
反应ⅡCO(g)+$\frac{1}{2}$O 2 (g)=CO 2 (g)△H=b kJ?mol -1 测得在不同温度下,K值如下:
①写出反应Ⅰ的K的表达式k=$\frac{C(CO)}{C(C{O}_{2})}$.
②反应Ⅰ中的a大于0(填大于、小于、等于).
③若500℃时进行反应Ⅰ,CO 2 起始浓度为2mol?L -1,CO的平衡浓度为1mol?L -1.
④700℃反应Ⅰ达到平衡,要使得该平衡向右移动,其它条件不变时,可以采取的措施有BC(填序号).
A.缩小反应器体积 B.通入CO 2
C.升高温度到900℃D.使用合适的催化剂
⑤由反应Ⅰ和Ⅱ可求得,反应2Fe(s)+O 2(g)=2FeO(s)的△H=2(a+b)kJ?mol -1.
(3)铁红是一种红色颜料,其成份是Fe2O3.将一定量的铁红溶于160mL 5mol•L-1盐酸中,再加入一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为11.2g.
(1)铁酸钠(Na 2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe 3+.
①铁酸钠中铁元素的化合价为+6.
②铁酸钠用于水处理,除了能消毒杀菌外,还可以像明矾【KAl(SO4)2】一样起到净水作用,请说明明矾的净水原理:Al3++3H2O?Al(OH)3+3H+.(用离子方程式表示)
(2)反应ⅠFe(s)+CO 2 (g)?FeO(s)+CO(g)△H=a kJ?mol -1,平衡常数为K;
反应ⅡCO(g)+$\frac{1}{2}$O 2 (g)=CO 2 (g)△H=b kJ?mol -1 测得在不同温度下,K值如下:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
②反应Ⅰ中的a大于0(填大于、小于、等于).
③若500℃时进行反应Ⅰ,CO 2 起始浓度为2mol?L -1,CO的平衡浓度为1mol?L -1.
④700℃反应Ⅰ达到平衡,要使得该平衡向右移动,其它条件不变时,可以采取的措施有BC(填序号).
A.缩小反应器体积 B.通入CO 2
C.升高温度到900℃D.使用合适的催化剂
⑤由反应Ⅰ和Ⅱ可求得,反应2Fe(s)+O 2(g)=2FeO(s)的△H=2(a+b)kJ?mol -1.
(3)铁红是一种红色颜料,其成份是Fe2O3.将一定量的铁红溶于160mL 5mol•L-1盐酸中,再加入一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为11.2g.
11.下列属于离子化合物的是( )
| A. | HCl | B. | N2 | C. | AlCl3 | D. | NH4Cl |
10.下列说法中,正确的是( )
0 158696 158704 158710 158714 158720 158722 158726 158732 158734 158740 158746 158750 158752 158756 158762 158764 158770 158774 158776 158780 158782 158786 158788 158790 158791 158792 158794 158795 158796 158798 158800 158804 158806 158810 158812 158816 158822 158824 158830 158834 158836 158840 158846 158852 158854 158860 158864 158866 158872 158876 158882 158890 203614
| A. | 分子中键的极性越强,分子越稳定 | |
| B. | 若把H2S写成H3S,违背了共价键的饱和性 | |
| C. | 分子中共价键的键能越大,键越长,则分子越稳定 | |
| D. | 分子中共价键的键能越大,该物质的性质越不活泼 |
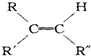 $→_{②Zn/H_{2}O}^{①O_{3}}$
$→_{②Zn/H_{2}O}^{①O_{3}}$ +
+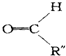 .
.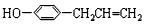 ,C
,C ,E
,E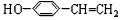 .
.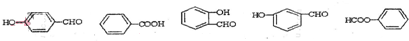 .
.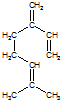 ,也可简写为
,也可简写为 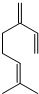 ,其分子式是C10H16,可以发生的化学反应有①④(选填序号).
,其分子式是C10H16,可以发生的化学反应有①④(选填序号).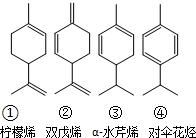
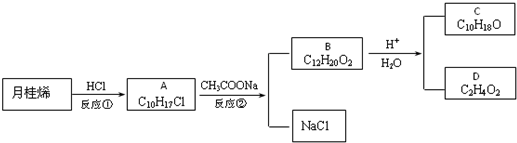
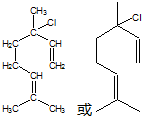 .
. .
.
 .
.
 ,A的晶体类型离子晶体.
,A的晶体类型离子晶体.