10.下列各种说法正确的是( )
①铝用于软包装是利用了铝密度小的物理性质
②在加热条件下,FeO可以迅速变成Fe2O3
③合金材料可能含有非金属元素
④合成纤维和光导纤维都是新型无机非金属材料
⑤高纯度的硅广泛用于制作计算机芯片
⑥不能用自来水直接配制AgNO3溶液
⑦粗铜精炼时,纯铜与外电源的正极相连
⑧在金属元素和非金属元素的分界线附近可以寻找制备半导体材料的元素.
①铝用于软包装是利用了铝密度小的物理性质
②在加热条件下,FeO可以迅速变成Fe2O3
③合金材料可能含有非金属元素
④合成纤维和光导纤维都是新型无机非金属材料
⑤高纯度的硅广泛用于制作计算机芯片
⑥不能用自来水直接配制AgNO3溶液
⑦粗铜精炼时,纯铜与外电源的正极相连
⑧在金属元素和非金属元素的分界线附近可以寻找制备半导体材料的元素.
| A. | 仅②③④⑤⑥⑧ | B. | 仅③⑤⑥⑧ | C. | 仅①②④⑦ | D. | 除①外 |
9.下列关于原电池和电解池的区别与联系的说法中,不正确的是( )
| A. | 原电池是将化学能转化为电能的装置,而电解池是将电能转化为化学能的装置 | |
| B. | 电解池的形成条件中要求必须有电源,原电池的形成条件中不要求有电源 | |
| C. | 原电池的负极和电解池的阴极发生的反应类型一样,都是氧化反应 | |
| D. | 原电池的正极和电解池的阴极都是电子流入的一极 |
8.下列措施不符合节能减排的是( )
| A. | 在屋顶安装太阳能热水器为居民提供生活用水 | |
| B. | 用石灰对煤燃烧后形成的烟气脱硫,并回收石膏 | |
| C. | 用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气作为家庭燃气 | |
| D. | 大力发展火力发电,解决广东电力紧张问题 |
3.下列用于解释实验事实的化学方程式正确的是( )
0 158691 158699 158705 158709 158715 158717 158721 158727 158729 158735 158741 158745 158747 158751 158757 158759 158765 158769 158771 158775 158777 158781 158783 158785 158786 158787 158789 158790 158791 158793 158795 158799 158801 158805 158807 158811 158817 158819 158825 158829 158831 158835 158841 158847 158849 158855 158859 158861 158867 158871 158877 158885 203614
| A. | Al2(SO4)3溶液滴加氨水产生白色胶状沉淀:Al3++3OH-=Al(OH)3↓ | |
| B. | 纯碱溶液使酚酞变红:CO32-+2H2O?H2CO3+2OH- | |
| C. | 乙酸清除水垢后的化学反应原理:2H++CO32-=CO2↑+H2O | |
| D. | FeCl3溶液中加入足量铁粉,溶液由黄色变成浅绿色:2Fe3++Fe=3Fe2+ |
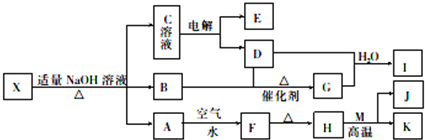
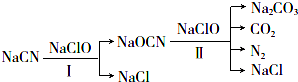
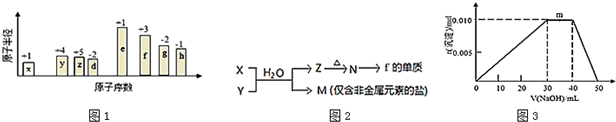
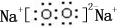 ;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)
;B是常见的液态化合物,其稀溶液易被催化分解,可使用的催化剂为AB.(填序号)