16.200℃时,11.6g CO2和H2O的混合物气体与足量的Na2O2反应,反应后固体增加了3.6g,则原混合物的平均相对分子质量为( )
| A. | 5.8 | B. | 11.6 | C. | 23.2 | D. | 36.4 |
12.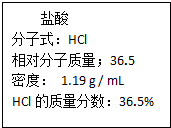 (I)表中①~⑥均是由Na、Mg、H、O、S、Cl等元素中的几种组成,根据物质的组成和性质将它们进行了分类.
(I)表中①~⑥均是由Na、Mg、H、O、S、Cl等元素中的几种组成,根据物质的组成和性质将它们进行了分类.
(1)表中物质②的化学式为HClO4;③的电子式为 .
.
(2)①的稀溶液和⑥的溶液反应的离子方程式为:2H++SO32-═H2O+SO2↑.
(II)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为:11.9mol/L.
(2)某学生欲用上述浓盐酸和蒸馏水配置500mL 物质的量浓度为0.400mol/L的稀盐酸.
①该学生需要量取16.8mL上述浓盐酸.
②实验中除合适的量筒、烧杯、玻璃棒外还需要的玻璃仪器有500mL容量瓶、胶头滴管.
③在配置过程中,下列实验操作对所配稀盐酸的物质的量浓度有何影响?(填“偏高”、“偏低”或无影响).
a.用量筒量取浓盐酸时俯视读数偏低.
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量蒸馏水偏低.
(3)①假设该同学成功配置了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的氢氧
化钠溶液,该同学需取25mL盐酸.
②该同学用新配置的盐酸中和含0.4g NaOH的氢氧化钠溶液,发现实际所用体积偏小,则可能
的原因是C.
A.盐酸挥发,浓度不足 B.配置过程中未洗涤烧杯和玻璃棒
C.配置溶液定容时,俯视容量瓶刻度线 D.加水超过刻度线,用胶头滴管吸出.
 (I)表中①~⑥均是由Na、Mg、H、O、S、Cl等元素中的几种组成,根据物质的组成和性质将它们进行了分类.
(I)表中①~⑥均是由Na、Mg、H、O、S、Cl等元素中的几种组成,根据物质的组成和性质将它们进行了分类.| 物质类别 | 含氧强酸 | 碱 | 钠盐 |
| 化学式 | ①H2SO4②HClO4 | ③ ④Mg(OH)2 ④Mg(OH)2 | ⑤NaCl ⑥Na2SO3 |
 .
.(2)①的稀溶液和⑥的溶液反应的离子方程式为:2H++SO32-═H2O+SO2↑.
(II)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为:11.9mol/L.
(2)某学生欲用上述浓盐酸和蒸馏水配置500mL 物质的量浓度为0.400mol/L的稀盐酸.
①该学生需要量取16.8mL上述浓盐酸.
②实验中除合适的量筒、烧杯、玻璃棒外还需要的玻璃仪器有500mL容量瓶、胶头滴管.
③在配置过程中,下列实验操作对所配稀盐酸的物质的量浓度有何影响?(填“偏高”、“偏低”或无影响).
a.用量筒量取浓盐酸时俯视读数偏低.
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量蒸馏水偏低.
(3)①假设该同学成功配置了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的氢氧
化钠溶液,该同学需取25mL盐酸.
②该同学用新配置的盐酸中和含0.4g NaOH的氢氧化钠溶液,发现实际所用体积偏小,则可能
的原因是C.
A.盐酸挥发,浓度不足 B.配置过程中未洗涤烧杯和玻璃棒
C.配置溶液定容时,俯视容量瓶刻度线 D.加水超过刻度线,用胶头滴管吸出.
11.设NA表示阿伏加德罗常数的值,下列叙述中一定正确的是( )
0 158684 158692 158698 158702 158708 158710 158714 158720 158722 158728 158734 158738 158740 158744 158750 158752 158758 158762 158764 158768 158770 158774 158776 158778 158779 158780 158782 158783 158784 158786 158788 158792 158794 158798 158800 158804 158810 158812 158818 158822 158824 158828 158834 158840 158842 158848 158852 158854 158860 158864 158870 158878 203614
| A. | 1 mol C4H10分子中共价键总数为13NA | |
| B. | 1L 1mol•L-1 盐酸中,含有HCl分子数为NA | |
| C. | 18g D2O 中含有的质子数和电子数均为10NA | |
| D. | 1molCl2与Fe 反应转移的电子数目为3NA |
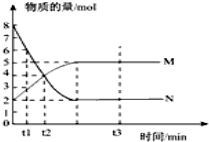 一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图示.
一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图示. 图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料.
图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料.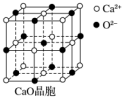 可以由下列反应合成三聚氰胺:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO↑,CaC2+N2$\frac{\underline{\;高温\;}}{\;}$CaCN2+C,CaCN2+2H2O═NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺.
可以由下列反应合成三聚氰胺:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO↑,CaC2+N2$\frac{\underline{\;高温\;}}{\;}$CaCN2+C,CaCN2+2H2O═NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺.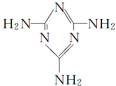 )俗称“蛋白精”,三聚氰酸(
)俗称“蛋白精”,三聚氰酸( 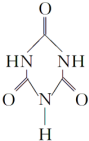 ).
).