9.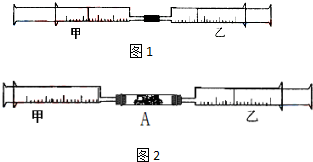 如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).
如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).
(1)如果实验1甲针筒内改装15mL Cl2,乙针筒内仍为40mL NH3,实验时,甲针筒内也有白烟产生.写出有关反应的化学方程式.3Cl2+8NH3=N2+6NH4Cl
(2)由实验2可知,常温常压下氯气在水中的溶解度为1体积水溶解2体积氯气.
(3)实验3 反应后甲针筒内气体的体积为15ml~30ml.
(4)实验4中,AlCl3溶液浓度为0.1mol/L,如果最后白色沉淀全部消失,则NaOH溶液浓度至少为0.8mol/L.
(5)将上述装置做以下改进:在甲、乙针筒之间连接一段硬质玻璃管,如图2.在A处装一种浅黄色的粉末,乙针筒内是一种常见的气体,甲针筒无气体.将乙针筒内气体压入甲针筒内,发现气体体积是原来的一半.A处的物质是Na2O2,甲针筒内的气体为O2.
(6)有学生用上述改进后的装置测定空气中氧气的体积分数(加热用酒精灯未画出).乙针筒内装有50mL空气.实验时,用酒精灯对A处物质进行加热,经反复慢慢推拉两针筒的活塞,反应完毕,恢复至室温,测得剩余气体为40.5mL.
1)A处的物质是c(选填编号).
a.碳粉 b.二氧化锰 c.铜粉 d.氧化铜
2)已知空气中氧气的体积分数为0.2,则该实验的相对误差为-5%.
 如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).
如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 40mL HCl | 40mL NH3 | 产生白烟 |
| 2 | 40mL Cl2 | 10mL 水 | 剩余气体为20mL |
| 3 | 30mL NO | 15mL O2 | |
| 4 | 20mL AlCl3溶液 | 10mL NaOH溶液 | 生成白色沉淀,后消失 |
(2)由实验2可知,常温常压下氯气在水中的溶解度为1体积水溶解2体积氯气.
(3)实验3 反应后甲针筒内气体的体积为15ml~30ml.
(4)实验4中,AlCl3溶液浓度为0.1mol/L,如果最后白色沉淀全部消失,则NaOH溶液浓度至少为0.8mol/L.
(5)将上述装置做以下改进:在甲、乙针筒之间连接一段硬质玻璃管,如图2.在A处装一种浅黄色的粉末,乙针筒内是一种常见的气体,甲针筒无气体.将乙针筒内气体压入甲针筒内,发现气体体积是原来的一半.A处的物质是Na2O2,甲针筒内的气体为O2.
(6)有学生用上述改进后的装置测定空气中氧气的体积分数(加热用酒精灯未画出).乙针筒内装有50mL空气.实验时,用酒精灯对A处物质进行加热,经反复慢慢推拉两针筒的活塞,反应完毕,恢复至室温,测得剩余气体为40.5mL.
1)A处的物质是c(选填编号).
a.碳粉 b.二氧化锰 c.铜粉 d.氧化铜
2)已知空气中氧气的体积分数为0.2,则该实验的相对误差为-5%.
8.下列实验所用试剂错误的是( )
| A. | 检验乙炔中是否混有H2S:湿润的醋酸铅试纸 | |
| B. | 盐酸滴定NaHCO3溶液:酚酞 | |
| C. | 检验淀粉是否完全水解:碘水 | |
| D. | 检验氯化氢是否集满:湿润的pH试纸 |
6.汽车尾气中的主要污染物是NO以及燃料不完全燃烧所产生的CO.为了减轻大气污染科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,即 2NO+2CO?2CO2+N2.
为了测定在某种催化剂作用下该反应的反应速率,t1℃下,在一等容的密闭容器中,用气体传感器测得了不同时间的NO和CO的浓度如表(CO2和N2的起始浓度为0).
回答下列问题:
(1)已知在上述反应中,反应物总能量大于生成物总能量,则正反应是放热反应(填“放热”或“吸热”).
(2)前3s内的平均反应速率:υ(N2)=1.42×10-4mol/(L•s).
(3)t1℃时该反应的平衡常数表达式:K=$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$.
(4)假设在密闭容器中该反应达到平衡后,改变下列条件,能提高NO转化率的是cd(选填答案编号).
a.选用更有效的催化剂 b.升高反应体系的温度
c.降低反应体系的温度 d.缩小容器的体积.
为了测定在某种催化剂作用下该反应的反应速率,t1℃下,在一等容的密闭容器中,用气体传感器测得了不同时间的NO和CO的浓度如表(CO2和N2的起始浓度为0).
| 时间 (s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (×10-4,mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO) (×10-3,mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
(1)已知在上述反应中,反应物总能量大于生成物总能量,则正反应是放热反应(填“放热”或“吸热”).
(2)前3s内的平均反应速率:υ(N2)=1.42×10-4mol/(L•s).
(3)t1℃时该反应的平衡常数表达式:K=$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$.
(4)假设在密闭容器中该反应达到平衡后,改变下列条件,能提高NO转化率的是cd(选填答案编号).
a.选用更有效的催化剂 b.升高反应体系的温度
c.降低反应体系的温度 d.缩小容器的体积.
4.为检验某化合物是否含碳、氢、氧三种元素,取一定质量该化合物在氧气中充分燃烧,接下来还须进行的实验有:①用带火星的木条检验氧气;②用无水硫酸铜检验是否有水生成;③用澄清石灰水检验是否有二氧化碳生成;④测定生成水和二氧化碳的质量.( )
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ②③ |
3.下列化学用语表示的是离子的有①H2O2②Si ③SO42-④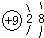 ⑤$\stackrel{+2}{M}g$( )
⑤$\stackrel{+2}{M}g$( )
0 158671 158679 158685 158689 158695 158697 158701 158707 158709 158715 158721 158725 158727 158731 158737 158739 158745 158749 158751 158755 158757 158761 158763 158765 158766 158767 158769 158770 158771 158773 158775 158779 158781 158785 158787 158791 158797 158799 158805 158809 158811 158815 158821 158827 158829 158835 158839 158841 158847 158851 158857 158865 203614
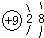 ⑤$\stackrel{+2}{M}g$( )
⑤$\stackrel{+2}{M}g$( )| A. | ①② | B. | ②④ | C. | ③④ | D. | ③⑤ |
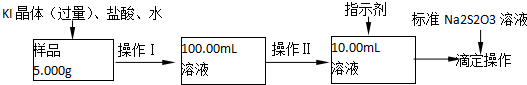
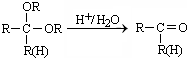
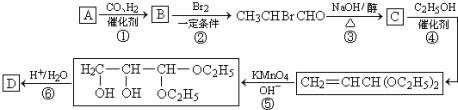
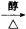 CH2=CHCHO+NaBr+H2O.
CH2=CHCHO+NaBr+H2O.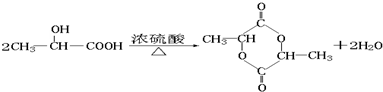 .
.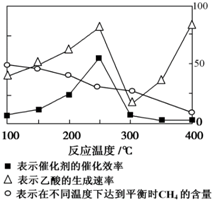 甲烷既是一种清洁能源,也是一种重要的化工原料.用催化剂可以将CO2和CH4直接转化成乙酸,反应方程式为:CO2(g)+CH4(g)?CH3COOH(g).
甲烷既是一种清洁能源,也是一种重要的化工原料.用催化剂可以将CO2和CH4直接转化成乙酸,反应方程式为:CO2(g)+CH4(g)?CH3COOH(g).