17.已知2Fe3++2I-=2Fe2++I2,Br2+2Fe2+=2Br-+2Fe3+.往含有FeBr2、FeI2的混合液中通入一定量的氯气后,再滴加少量的KSCN溶液,溶液变为红色,则下列说法不正确的是( )
| A. | 按I-、Fe2+、Br-的顺序还原性逐渐减弱 | |
| B. | 通入氯气后原溶液中Fe2+一定被氧化 | |
| C. | 原溶液中Br-一定被氧化 | |
| D. | 不能确定通入氯气后的溶液中是否还存在Fe2+ |
16.下列说法正确的是( )
| A. | 足量的KI溶液与FeCl3溶液反应后,用CCl4萃取其中的I2,分液,在水溶液中滴加KSCN溶液仍呈血红色,说明该反应有一定的限度 | |
| B. | 在一定条件下,一份双氧水样品经过2h,H2O2的浓度从0.05mol•L-1下降到0.03 mol•L-1,该双氧水在这2h中分解的平均反应速率约为0.015 mol•L-1•h-1 | |
| C. | 其它条件相同时,反应温度升高,对于吸热反应,反应速率加快,对于放热反应,反应速率减慢 | |
| D. | 一定条件下,固定体积的容器中发生反应A(g)+B(g)?2C(g),当容器内A、B、C的浓度之比为1:1:2时,该反应一定处于平衡状态 |
15.下列说法正确的是( )
| A. | CaCl2晶体中存在共价键 | |
| B. | H2SO4溶于水能电离出H+和SO42-,所以硫酸是离子化合物 | |
| C. | SiO2属于原子晶体,熔化破坏共价键和分子间作用力 | |
| D. | I2是分子晶体,加热升华过程中只需克服分子间作用力 |
14.某可逆反应过程的能量变化如图所示,下列说法正确的是( )
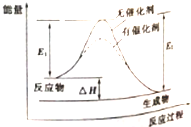

| A. | 该反应能量变化类型与CaCO3分解反应相同 | |
| B. | 加催化剂后,正反应速率加快,逆反应速率减小 | |
| C. | 若该反应为氧化还原反应,则可以将其设计成原电池 | |
| D. | 反应热△H=E2-E1 |
13.下列说法正确的是( )
| A. | 在紫外线、饱和Na2SO4、CuSO4溶液、福尔马林等作用下,蛋白质均会发生变性 | |
| B. | 油脂属于高分子化合物,是混合物 | |
| C. | 在一定条件下,氨基酸之间能发生反应,合成更加复杂的化合物 | |
| D. | 检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热,观察是否有砖红色沉淀 |
12.下列说法正确的是( )
| A. | 煤、石油、沼气属于人类利用的主要化石燃料 | |
| B. | 煤干馏是复杂的物理化学变化,可得到焦炭、煤焦油和焦炉煤气等 | |
| C. | 氢气是一种清洁能源 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
11.下列物质的水溶液因水解而呈碱性的是( )
| A. | NaOH | B. | (NH4)2SO4 | C. | Na2O | D. | CH3COONa |
10.下列仪器对应名称正确的是( )
0 158652 158660 158666 158670 158676 158678 158682 158688 158690 158696 158702 158706 158708 158712 158718 158720 158726 158730 158732 158736 158738 158742 158744 158746 158747 158748 158750 158751 158752 158754 158756 158760 158762 158766 158768 158772 158778 158780 158786 158790 158792 158796 158802 158808 158810 158816 158820 158822 158828 158832 158838 158846 203614
| A. |  容量瓶 | B. |  蒸馏烧瓶 | C. |  蒸发皿 | D. |  滴定管 |
 .
.