8.关于金属腐蚀和防护原理的叙述中,错误的是( )
| A. | 埋在地下的钢管与电源负极连接可以减缓腐蚀 | |
| B. | 原电池负极和电解池阳极发生的都是氧化反应 | |
| C. | 钢铁析氢腐蚀的正极反应:2H++2e→H2↑ | |
| D. | 为了避免青铜器生成铜绿,将青铜器放在银质托盘上 |
7.下列混和物可用分液漏斗分离的是( )
| A. | 苯和植物油 | B. | 乙酸乙酯与饱和碳酸钠溶液 | ||
| C. | 甘油和水 | D. | 苯和液溴 |
6.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | c(SO32-)=0.5 mol•L-1的溶液中:ClO-、Na+、Cl-、CO32- | |
| B. | pH=1的溶液中:NH4+、Na+、SO42-、Fe3+ | |
| C. | 强碱性溶液中:Na+、AlO2-、NO3-、HCO3- | |
| D. | 水电离产生的c(H+)=1×10-14mol•L-1的溶液中:HCO3-、NH4+、Cl-、Ca2+ |
5.下列实验目的可以达到的是( )
| A. | 将滴有稀硫酸的淀粉溶液加热后,加入新制的Cu(OH)2悬浊液,加热,没有红色沉淀,说明淀粉在该条件下没有水解 | |
| B. | 将铜与足量的浓硝酸反应生成的气体干燥后收集,用冰水混合物冷却降温,研究温度对化学平衡的影响 | |
| C. | 将混合气体通过饱和Na2CO3溶液以便除去CO2中少量的SO2 | |
| D. | 某无色溶液中加入Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
4.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 0oC,1.01×106Pa时,11.2L氧气所含的氧原子数为NA | |
| B. | 标准状况下,80gSO3所占的体积约为22.4L | |
| C. | 31g白磷分子中,含有的共价单键数目是NA | |
| D. | 0.5 mol Na2O2中含有的阴离子数为0.5NA |
3.下列有关表述正确的是( )
| A. | N原子的价电子轨道表示式: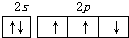 | |
| B. | 碳酸氢钠在水溶液中的电离方程式:NaHCO3?Na++H++CO32- | |
| C. | 羧基的结构式: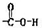 | |
| D. | 明矾的化学式为 KAlSO4•12H2O |
2.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 垃圾是放错地方的资源,应分类回收利用 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 实现化石燃料清洁利用,就无需开发新能源 | |
| D. | 为提高农作物的产量和质量,应大量使用化肥和农药 |
20.一定量饱和Na2CO3溶液中逐滴加入稀盐酸直至过量,开始阶段无现象,后来冒气泡.以下判断错误的是( )
| A. | CO32-离子是弱酸根,开始阶段与H+结合,生成HCO3- | |
| B. | 溶液中的Na+、Cl-抑制了CO2生成 | |
| C. | 开始生成的CO2与Na2CO3反应,生成了NaHCO3 | |
| D. | CO32-离子在水中,存在两个水解平衡,开始阶段可能是H+结合OH-,生成HCO3- |
19.一定温度下,测定某溶液中只含NH4+、Cl-、H+、OH-四种离子,下列说法一定正确的是( )
0 158647 158655 158661 158665 158671 158673 158677 158683 158685 158691 158697 158701 158703 158707 158713 158715 158721 158725 158727 158731 158733 158737 158739 158741 158742 158743 158745 158746 158747 158749 158751 158755 158757 158761 158763 158767 158773 158775 158781 158785 158787 158791 158797 158803 158805 158811 158815 158817 158823 158827 158833 158841 203614
| A. | 溶液中四种粒子之间满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| B. | 若溶液中粒子间满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中溶质为:NH3•H2O和NH4Cl | |
| C. | 若溶液中粒子间满足:c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中溶质只有NH4Cl | |
| D. | 若溶液中c(NH4+)=c(Cl-),则该溶液pH等于7. |