5.设NA表示阿伏加德罗常数,下列说法中错误的是( )
| A. | 常温常压下,22.4L氮气所含分子数小于NA个 | |
| B. | 1molCl2通入足量水中电子转移数为NA个 | |
| C. | 1molSiO2中含有4 molSi-O键 | |
| D. | 12g金刚石含有NA个碳原子 |
4.A与B在溶液中进行反应,无论A与B的物质的量之比如何,都可以用所示的离子方程式表示的是( )
| A. | 碘化钾与氯气:5I-+3Cl2-+3H2O→IO3-+6Cl-+6H+ | |
| B. | KAl(SO4)2与Ba(OH)2:2Ba2++4OH-+Al3++2SO42-→2BaSO4↓+AlO2-+2H2O | |
| C. | 氨水与SO2:NH3•H2O+SO2→HSO3-+NH4+ | |
| D. | NaAlO2与AlCl3:Al3++3AlO2-+6H2O→4Al (OH)3↓ |
3.炼钢时,将氧气、生石灰加入熔融生铁后,会发生多个反应,其中不可能生成的是( )
| A. | CaSiO3 | B. | Ca3(PO4)2 | C. | Fe2O3 | D. | CO |
2.某原电池的总反应为:2FeCl3+Fe→3FeCl2,则以下叙述正确的是( )
| A. | 铁作阳极 | B. | 炭棒作阴极 | ||
| C. | 正极反应式为Fe3++e-→Fe2+ | D. | 负极反应式为Fe2+-e-→Fe3+ |
1.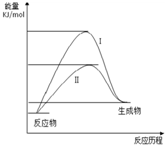 某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )
某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )
 某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )
某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )| A. | 反应物的状态 | B. | 反应的完成程度 | C. | 生产能耗 | D. | 反应热效应 |
20.以下不能比较硫和磷非金属性相对强弱的是( )
| A. | 单质的活泼性 | B. | 氢化物的稳定性 | ||
| C. | H-S键和H-P键的极性 | D. | 最高氧化物对应水化物的酸性 |
19.下列有关实验设计或对实验原理的描述正确的是( )
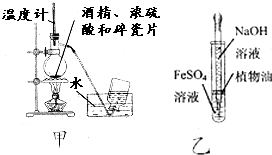

| A. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体 | |
| B. | 用甲图装置制取乙烯 | |
| C. | 用乙图装置制备少量氢氧化亚铁 | |
| D. | 加入适量乙醇和浓硫酸,加热,可除去乙酸乙酯中少量的乙酸 |
18.下列说法正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | H2O、D2O、T2O互为同分异构体 | |
| C. | CH4、CCl4都是含有极性键的非极性分子 | |
| D. | HF、HCl、HBr、HI的稳定性依次增强 |
17.久置空气中会发生颜色变化,但颜色变化不是由于跟氧气反应引起的是( )
| A. | 过氧化钠固体 | B. | 苯酚晶体 | C. | 硫酸亚铁晶体 | D. | 亚硫酸钠固体 |
16.关于物质的检验,下列判断正确的是( )
0 158632 158640 158646 158650 158656 158658 158662 158668 158670 158676 158682 158686 158688 158692 158698 158700 158706 158710 158712 158716 158718 158722 158724 158726 158727 158728 158730 158731 158732 158734 158736 158740 158742 158746 158748 158752 158758 158760 158766 158770 158772 158776 158782 158788 158790 158796 158800 158802 158808 158812 158818 158826 203614
| A. | 在溶液中加入盐酸酸化,无现象;再加入BaCl2溶液,如果生成白色沉淀,则原溶液中一定有大量的SO42-存在 | |
| B. | 在溶液中加入AgNO3溶液,生成不溶于硝酸的沉淀,则原溶液中一定有Cl-存在 | |
| C. | 在溶液中加入浓NaOH溶液,加热后如果生成气体使湿润的红色石蕊试纸变蓝,则原溶液一定是铵盐溶液 | |
| D. | 在溶液中加入KSCN溶液,无现象;再加入稀硝酸,溶液变血红色,则原溶液中一定有Fe2+存在 |