5.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 30 g乙烷中所含的极性共价键数为7NA | |
| B. | 标准状况下,22.4 L N2和CO2混合气体所含的分子数为2NA | |
| C. | 已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,则NA个N2分子与足量氢气充分反应释放热量92.4kJ | |
| D. | Na2O2与CO2反应生成1 molO2时,转移的电子数为2NA |
4.除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 甲烷(甲醛) | 银氨溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
3.下列有关铁的叙述错误的是( )
| A. | 铁的熔点比生铁要高 | |
| B. | 不能通过化合反应制得FeC12 | |
| C. | 地壳中含量铝比铁高,但在我国使用上铁比铝历史悠久 | |
| D. | Fe3O4既可以是铁与氧气反应的产物也可以是铁与水蒸气反应的产物 |
1.N2O5是一种新型硝化剂,在一定条件下可发生下列反应:2N2O5 (g)?4NO2(g)+O2 (g)-Q(Q>0)
(1)如果上述反应在恒容密闭容器中发生,下列能说明反应达到平衡状态的是ac(选填编号).
a.2v正(N2O5)=v逆(NO2) b.v(NO2)=4v(O2)
c.O2的物质的量的分数保持不变 d.混合气体的密度保持不变
e.每消耗1mol N2O5的同时生成2mol NO2
(2)表为在2L的恒容密闭容器中,反应在T1温度下的部分实验数据:
则500s内N2O5的分解速率为2.96×10-3mol/(L•s).
(3)若其它条件不变,将温度由T1改变到T2,反应1000s时测得,n( NO2)为9.96mol,则T2<T1(选填“>”、“<”或“=”).
(4)达到平衡后,若其它条件不变,瞬间压缩容器体积至原来的一半,则NO2浓度的变化情况为NO2浓度大于原浓度,小于原浓度的2倍.
(1)如果上述反应在恒容密闭容器中发生,下列能说明反应达到平衡状态的是ac(选填编号).
a.2v正(N2O5)=v逆(NO2) b.v(NO2)=4v(O2)
c.O2的物质的量的分数保持不变 d.混合气体的密度保持不变
e.每消耗1mol N2O5的同时生成2mol NO2
(2)表为在2L的恒容密闭容器中,反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| n(N2O5)/mol | 10.0 | 7.04 | 4.96 |
(3)若其它条件不变,将温度由T1改变到T2,反应1000s时测得,n( NO2)为9.96mol,则T2<T1(选填“>”、“<”或“=”).
(4)达到平衡后,若其它条件不变,瞬间压缩容器体积至原来的一半,则NO2浓度的变化情况为NO2浓度大于原浓度,小于原浓度的2倍.
20.25℃时,将浓度和体积分别为c1、V1的一元强碱ROH溶液和c2、V2的一元弱酸HA溶液相混合,下列关于该混合溶液的叙述正确的是( )
| A. | 若pH>7时,则一定是c1V1=c2V2 | |
| B. | 只有当pH<7时,才能满足c(R+)+c(H+)=c(A-)+c(OH-) | |
| C. | 当pH=7时,若V1=V2,则一定是c1<c2 | |
| D. | 若V1=V2、c1=c2,则c(A-)+c(HA)=c(R+) |
19.在“绿色化学工艺”中,理想状态是原子利用率为100%.在用CH3C≡CH合成CH2=C(CH3)COOCH3的过程中,欲使原子利用率达到最高,还需要的其它反应物有( )
| A. | CO和CH3OH | B. | CO2和H2O | C. | H2和CO2 | D. | CH3OH和H2 |
18. 科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
 科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )| A. | 石墨烯是一新型的纳米化合物 | B. | 石墨烯与C60互为同素异形体 | ||
| C. | 石墨烯是一种有机物 | D. | 石墨烯中碳元素的化合价为+3 |
17.根据表提供的数据,下列判断正确的是( )
| 化学式 | 电离常数 |
| HF | Ki=3.5×10-4 |
| H2CO3 | Ki1=4.3×10-7 |
| Ki2=5.6×10-11 | |
| HClO | Ki=3.2×10-8 |
| A. | 同温同浓度下,溶液的pH值:NaF>NaClO>Na2CO3 | |
| B. | 结合H+的能力:ClO->HCO3->F- | |
| C. | 次氯酸钠溶液中通少量二氧化碳的离子方程式:ClO-+CO2+H2O→HCO3-+HClO | |
| D. | 碳酸钠溶液中加入少量氢氟酸的离子方程式:CO32-+2HF→2F-+H2O+CO2↑ |
16.对于0.1mol/L Na2SO3溶液,下列叙述正确的是( )
0 158628 158636 158642 158646 158652 158654 158658 158664 158666 158672 158678 158682 158684 158688 158694 158696 158702 158706 158708 158712 158714 158718 158720 158722 158723 158724 158726 158727 158728 158730 158732 158736 158738 158742 158744 158748 158754 158756 158762 158766 158768 158772 158778 158784 158786 158792 158796 158798 158804 158808 158814 158822 203614
| A. | c(Na+):c(SO32-)<2:1 | |
| B. | c(Na+)=2 c(SO32-)+c(HSO3-)+c(H2SO3) | |
| C. | c(Na+)+c(H+)=2 c(SO32-)+2 c(HSO3-)+c(OH-) | |
| D. | 加入少量NaOH固体,c(SO32-) 与c(Na+) 均增大 |
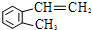 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.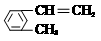 .
.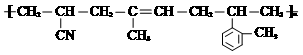 (假设按1:1:1的单体比例合成).
(假设按1:1:1的单体比例合成).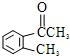 ,写出相关的化学方程式:
,写出相关的化学方程式: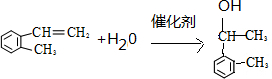 、
、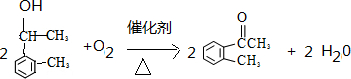 .
.