3.某同学进行中和反应实验:取适量的NaOH溶液于烧杯中,滴加几滴紫色石蕊试液.再逐渐滴加稀H2SO4测得溶液的pH及颜色变化情况如表:
(1)图中符合上述实验过程的图形是C

(2)当加人4ml稀H2SO4时,溶液显中性,溶液中的溶质为硫酸钠
(3)写出该中和反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.
| 滴加稀H2SO4的体积ml | O | l | 2 | 3 | 4 | 5 | 6 | 7 |
| pH | 13.0 | 12.8 | 12.5 | 12.2 | 7.0 | 2.0 | 1.7 | 1.6 |
| 溶液颜色 | 蓝色 | 紫色 | 红色 | |||||

(2)当加人4ml稀H2SO4时,溶液显中性,溶液中的溶质为硫酸钠
(3)写出该中和反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.
1.有M、N、P、Q四块金属片,进行如下实验:
①M、N用导线相连后,同时插入稀H2SO4中,M极为负极
②P、Q用导线相连后,同时浸入稀H2SO4中,电子由P→导线→Q
③M、P相连后,同时浸入稀H2SO4,P极产生大量气泡
④N、Q相连后,同时浸入稀H2SO4中,Q极发生氧化反应
由此判断四种金属的活动性顺序为( )
①M、N用导线相连后,同时插入稀H2SO4中,M极为负极
②P、Q用导线相连后,同时浸入稀H2SO4中,电子由P→导线→Q
③M、P相连后,同时浸入稀H2SO4,P极产生大量气泡
④N、Q相连后,同时浸入稀H2SO4中,Q极发生氧化反应
由此判断四种金属的活动性顺序为( )
| A. | M>P>Q>N | B. | P>M>N>Q | C. | N>Q>P>M | D. | M>N>P>Q |
1.已知氧化性:Br2>Fe3+>I2,向含溶质amolFeI2的溶液中加入含bmolBr2的溴水,充分反应.下列说法不正确的是( )
| A. | 离子的还原性强弱:I->Fe2+>Cl- | |
| B. | 当a≥b时,发生的离子反应:2I-+Br2=I2+2Br- | |
| C. | 当5a=4b时,反应后的离子浓度之比:c(Fe2+):c(Fe3+):c(Br-)=1:1:5 | |
| D. | 当3a≤2b时,发生的离子反应:2Fe2++2I-+2Br2=2Fe3++I2+4Br- |
20.目前,已经合成了LiH、NaH、CaH2、MgH2(AlH3)n等,下列说法不正确的是( )
| A. | 金属氢化物都是强还原剂 | |
| B. | 金属与H2制备金属氢化合物时,H2作还原剂 | |
| C. | 金属氢化物与水反应生成对应的碱和H2 | |
| D. | 离子半径:r(H-)>r(Li+) |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 19g H3O+共用的电子对数为2NA | |
| B. | 常温下,1L0.1mol/L AlCl3溶液中阳离子数小于0.1NA | |
| C. | 标准状况下,1.4gN2和CO的混合气体中含有的电子数为0.7NA | |
| D. | 200mL2.5mol/L乙醇溶液中含有的分子总数为0.5NA |
17.下列说法正确的是( )
0 158624 158632 158638 158642 158648 158650 158654 158660 158662 158668 158674 158678 158680 158684 158690 158692 158698 158702 158704 158708 158710 158714 158716 158718 158719 158720 158722 158723 158724 158726 158728 158732 158734 158738 158740 158744 158750 158752 158758 158762 158764 158768 158774 158780 158782 158788 158792 158794 158800 158804 158810 158818 203614
| A. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2-3次 | |
| B. | 向酒精灯内添加酒精时,不能多于容积的$\frac{2}{3}$,若不慎洒出的酒精在桌上燃烧,应迅速用水灭火 | |
| C. | 探究温度对反应速率的影响时,应先将硫代硫酸钠溶液、硫酸溶液分别在水浴中加热,然后混合 | |
| D. | 配制浓硫酸和浓硝酸的混合酸时,将浓硝酸沿器壁慢慢加入浓硫酸中,并不断搅拌 |
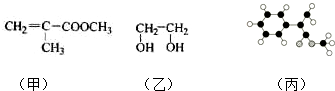

 ;
;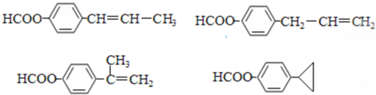 (只写一种即可)
(只写一种即可)