16.
(1)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥的后面.
(2)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4(或HNO3、H2CO3) | ③NaOH(或KOH) ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2SO4(或K2CO3、Na2SO3) | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(2)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
13.有机化学反应种类比较多,常见的有:①卤代反应 ②烯烃水化反应 ③氧化反应④还原反应 ⑤硝化反应 ⑥水解反应 ⑦酯化反应 ⑧消去反应 ⑨加聚反应⑩缩聚反应等等.其中属于取代反应的是( )
| A. | ①⑤⑥⑦ | B. | ②③④⑧⑨⑩ | C. | ①②⑤⑥⑦ | D. | ①⑤⑥⑦⑨⑩ |
11.下列各组物质中,所含原子个数相同的是( )
| A. | 9g水和0.75mol一氧化碳 | B. | 10g氢气和10g氧气 | ||
| C. | 22.4mL氢气(标况)和0.1mol氮气 | D. | 22g二氧化碳和16.8L溴单质(Br2) |
10.下列化学用语不正确的是( )
| A. | CO2的结构式:O=C=O | B. | 乙醇分子的球棍模型: | ||
| C. | Cl-结构示意图: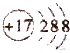 | D. | 四氯化碳的电子式: |
9. 某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊.A受热分解的化学方程式为2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复到室温,向所得溶液中各滴入2滴酚酞溶液.
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论:同温度下,Na2CO3比NaHCO3易溶于水.
②同学们在两烧杯中还观察到以下现象.其中,盛放Na2CO3的烧杯中出现的现象是bd(填字母序号).
a.溶液温度下降b.溶液温度升高c.滴入酚酞后呈浅红色d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中.
①两试管中均产生气体,Ⅰ(填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈.
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是ac(填字母序号).
a.装置Ⅰ的气球体积较大b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成0.5mol•L-1的溶液,设计如下方案并对反应现象做出预测:
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体,则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为Ca2++2HCO3-=CaCO3↓+CO2↑+H2O.
 某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊.A受热分解的化学方程式为2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复到室温,向所得溶液中各滴入2滴酚酞溶液.
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论:同温度下,Na2CO3比NaHCO3易溶于水.
②同学们在两烧杯中还观察到以下现象.其中,盛放Na2CO3的烧杯中出现的现象是bd(填字母序号).
a.溶液温度下降b.溶液温度升高c.滴入酚酞后呈浅红色d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中.
①两试管中均产生气体,Ⅰ(填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈.
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是ac(填字母序号).
a.装置Ⅰ的气球体积较大b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成0.5mol•L-1的溶液,设计如下方案并对反应现象做出预测:
| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2mL Na2CO3溶液中滴加1mL 0.5mol•L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应::Ca2++CO32-=CaCO3↓(写离子方程式) |
| 操作2:向2mL NaHCO3溶液中滴加1mL 0.5mol•L-1 CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应 |
8.下表为某轻质纯碱产品说明书:
其中有错误的一项是( )
 | 化学名:碳酸钠,俗称苏打 |
| 性状:白色粉末,易溶于水,水溶液呈中性 | |
| 化学式:Na2CO3 | |
| 用途:重要的基本化工原料之一,在纺织、玻璃、制皂、造纸等领域都有广泛应用 |
| A. | 化学名 | B. | 性状 | C. | 化学式 | D. | 用途 |
7.将等物质的量的H2SO4与NaOH溶液混合后,滴入紫色石蕊试液,溶液呈( )
0 158611 158619 158625 158629 158635 158637 158641 158647 158649 158655 158661 158665 158667 158671 158677 158679 158685 158689 158691 158695 158697 158701 158703 158705 158706 158707 158709 158710 158711 158713 158715 158719 158721 158725 158727 158731 158737 158739 158745 158749 158751 158755 158761 158767 158769 158775 158779 158781 158787 158791 158797 158805 203614
| A. | 紫色 | B. | 红色 | C. | 蓝色 | D. | 无色 |
 (1)写出工业上分别以①CH2=CH2为原料和②C6H12O6为原料制取乙醇的化学方程式:①CH2=CH2+H2O$→_{高温高压}^{催化剂}$CH3CH2OH②C6H12O6$\stackrel{催化剂}{→}$2CO2↑+2CH3CH2OH
(1)写出工业上分别以①CH2=CH2为原料和②C6H12O6为原料制取乙醇的化学方程式:①CH2=CH2+H2O$→_{高温高压}^{催化剂}$CH3CH2OH②C6H12O6$\stackrel{催化剂}{→}$2CO2↑+2CH3CH2OH