8. 央视曝光了双汇在食品生产中使用“瘦肉精”,一时间,市场哗然.瘦肉精的结构简式如图,下列有关说法错误的是( )
央视曝光了双汇在食品生产中使用“瘦肉精”,一时间,市场哗然.瘦肉精的结构简式如图,下列有关说法错误的是( )
 央视曝光了双汇在食品生产中使用“瘦肉精”,一时间,市场哗然.瘦肉精的结构简式如图,下列有关说法错误的是( )
央视曝光了双汇在食品生产中使用“瘦肉精”,一时间,市场哗然.瘦肉精的结构简式如图,下列有关说法错误的是( )| A. | 该有机物的核磁共振氢谱图中有6个吸收峰 | |
| B. | 该有机物的分子式为C12H18N2Cl2O | |
| C. | 该有机物能溶于水,且水溶液显碱性 | |
| D. | 该有机物能发生加成反应、取代反应、氧化反应和酯化反应 |
7.为提纯下列物质,所选除杂试剂和分离的主要操作方法都合理的是( )
| 选项 | 被提纯的物质(杂质) | 除杂试剂 | 主要操作方法 |
| A | NaHCO3溶液(Na2CO3) | 澄清石灰水 | 过滤 |
| B | NaCl溶液(Br2) | 乙醇 | 分液 |
| C | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
| D | KNO3溶液(KOH) | FeCl3溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
6.下列实验装置及操作不能达到实验目的是( )
| A. |  用Ca(OH)2和NH4Cl制取NH3 | B. |  从碘水中提取碘单质 | ||
| C. |  从食盐水中获取氯化钠 | D. |  用自来水制取蒸馏水 |
5.向某密闭容器中充入1mol CO和2mol H2O(g),发生反应CO+H2O(g)$?_{△}^{催化剂}$CO2+H2当反应达到平衡时,CO的体积分数为x.若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数小于x的是( )
| A. | 0.5mol CO+2mol H2O(g)+1mol CO2+1mol H2 | |
| B. | 1mol CO+1mol H2O(g)+1mol CO2+1mol H2 | |
| C. | 0.5mol CO+1.5mol H2O(g)+0.4mol CO2+0.4molH2 | |
| D. | 0.5mol CO+1.5mol H2O(g)+0.5molCO2+0.5mol H2 |
4.某溶液仅含 Fe2+?Na+?Al3+?Ba2+?SO42-?NO3-?Cl-中的4种离子,所含离子的物质的量均为1mol,若向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)?下列说法不正确的是
( )
( )
| A. | 该溶液中所含的离子是:Fe2+?Na+?SO42-?NO3-? | |
| B. | 若向该溶液中加入过量的稀硫酸,产生的气体在空气中能变成红棕色 | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 若向该溶液中加入足量的NaOH 溶液,充分反应后,过滤?洗涤?灼烧,最终所得固体的质量为72g |
3.在固定容积的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g),已知反应过程某一时刻SO2、O2、SO3浓度分别为0.2mol•L-1、0.1mol•L-1、0.2mol•L-1,达到平衡时浓度可能正确的是( )
| A. | SO2为0.3 mol•L-1 | |
| B. | SO2、O2分别为0.4 mol•L-1、0.2 mol•L-1 | |
| C. | SO2、SO3均为0.25 mol•L-1 | |
| D. | SO2、SO3分别为0.24 mol•L-1、0.14 mol•L-1 |
2.在1L密闭容器中通入2mol氨气,在一定温度下发生反应;2NH3?N2+3H2,达平衡时,N2的物质的量分数为a%,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a%的是( )
| A. | 6mol H2和2mol N2 | |
| B. | 2mol NH3和1mol N2 | |
| C. | 2mol N2和3mol H2 | |
| D. | 0.1mol NH3、0.95mol N2、2.85mol H2 |
1.CoO是电子陶瓷所需的重要原料,工业上可用含有Co2O3、Fe2O3、Li和Al等物质的废料制备CoO.生产流程如图:

已知:①Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
(1)为提高碱溶速率,除适当增大NaOH溶液浓度、提高反应温度外,还可采取的措施有将废料研磨成更小颗粒.
(2)步骤Ⅱ中酸溶时发生了反应:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O,此反应的目的是溶解Co2O3,将三价钴转化为Co2+,便于沉淀除去Fe3+.
(3)步骤Ⅲ中加入Na2CO3溶液的作用是调节溶液的pH,物质X的化学式为Fe(OH)3.
(4)步骤Ⅲ中加入NaF对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅵ中产生Li2CO3沉淀.
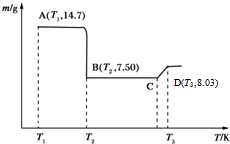
(5)操作A的步骤为过滤、洗涤、干燥,将所得的草酸钴晶体高温灼烧,其热重分析图如图:写出B点物质的化学式:CoO,CD段发生反应的化学方程式为:6CoO+O2=2Co3O4.
0 158568 158576 158582 158586 158592 158594 158598 158604 158606 158612 158618 158622 158624 158628 158634 158636 158642 158646 158648 158652 158654 158658 158660 158662 158663 158664 158666 158667 158668 158670 158672 158676 158678 158682 158684 158688 158694 158696 158702 158706 158708 158712 158718 158724 158726 158732 158736 158738 158744 158748 158754 158762 203614

已知:①Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(2)步骤Ⅱ中酸溶时发生了反应:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O,此反应的目的是溶解Co2O3,将三价钴转化为Co2+,便于沉淀除去Fe3+.
(3)步骤Ⅲ中加入Na2CO3溶液的作用是调节溶液的pH,物质X的化学式为Fe(OH)3.
(4)步骤Ⅲ中加入NaF对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅵ中产生Li2CO3沉淀.
(5)操作A的步骤为过滤、洗涤、干燥,将所得的草酸钴晶体高温灼烧,其热重分析图如图:写出B点物质的化学式:CoO,CD段发生反应的化学方程式为:6CoO+O2=2Co3O4.
