16.在100mL浓度为1mol/L的NaOH溶液中,通入1.68L SO2 气体(标况)后,在溶液中存在的溶质是( )
| A. | Na2SO3 和NaHSO3 | B. | Na2SO3 和NaOH | C. | Na2SO3 | D. | NaHSO4 |
15.下列变化中需要加入还原剂才能发生的是( )
| A. | N2→NO | B. | N2→NH3 | C. | NO→NO2 | D. | NH3→NO |
14.对于可逆反应M+N?P+Q,有关说法正确的是( )
| A. | 当达到了该反应的限度时,正、逆反应的速率为零 | |
| B. | 各物质的浓度不再发生变化时,则达到化学反应的限度 | |
| C. | 升高反应的温度,则反应速率减慢 | |
| D. | 使用催化剂,能改变反应限度 |
13.下列保存物质的方法正确的是( )
| A. | 液氯贮存在干燥的钢瓶里 | |
| B. | 少量的锂、钠、钾均保存在煤油中 | |
| C. | 氢氧化钠溶液保存在玻璃塞的细口瓶中 | |
| D. | 用排水法收集满一瓶氢气,瓶口朝上放置 |
12.下列实验操作中,不正确的是( )
| A. | 用四氯化碳萃取碘水中的碘单质 | |
| B. | 蒸馏时,冷却水从冷凝管的下口通入,上口流出 | |
| C. | 用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出 | |
| D. | 分离油和水的混合物需要萃取,分液 |
11.东汉成书的《神农本草经》有“石胆能化铁为铜”的记载(石胆是硫酸铜).这一方法开创了人类文明史上湿法冶金的先河.其中涉及到的化学反应类型是( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
10.下列说法错误的是( )
| A. | 向苦卤(含K+、Mg2+、Br-等)中通入Cl2是为了提取溴 | |
| B. | 粗盐(含Ca2+、Mg2+、SO42-、泥沙等杂质)可采用除杂和重结晶等过程提纯 | |
| C. | 海带提碘只涉及物理变化,海水提镁涉及复分解反应 | |
| D. | 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |
8.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 1molOH-和1mol羟基(-OH)所含电子数均为10NA | |
| B. | 56g铁与稀HNO3充分反应,转移电子数可能为3NA | |
| C. | 标准状态下,22.4LC4H6中含有碳碳三键数一定为NA | |
| D. | 将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积约为22.4L |
7.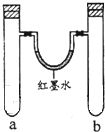 某化学小组用以下装置做兴趣实验(试管中有空气存在).
某化学小组用以下装置做兴趣实验(试管中有空气存在).
(1)实验1,同时加入试剂,反应开始可观察到U形管中液面b(填编号),简述产生该现象的原因钠与水反应比钠与乙醇反应快,所以开始时a试管中产生的氢气比b试管多,故液面应左低右高.
a.左高右低b.左低右高c.左右相平d.来回震荡
(2)写出钠与乙醇反应的化学方程式2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;反应结束静置一段时间,最终U形管中液面c(填题(1)编号).
(3)实验2,U形管中液面a(填题(1)编号);写出a试管中发生还原反应的电极反应方程式O2+2H2O+4e→4OH-.
(4)实验3,U形管中液面左低右高,检验b管中生成新物质的操作是取样,加入KSCN溶液,溶液变红,说明有Fe3+生成.
(5)其他条件不变情况下,将实验4a、b试管中硝酸同时改为3mLcd(填编号),即可观察到U形管液面产生相反现象.
a.无水乙醇b.浓硫酸c.稀硫酸d.浓盐酸
(6)常温下,在a、b试管中分别加入等体积的同种溶液,仅对a试管进行强光照射,一段时间后观察到U型管液面左低右高,根据所学知识,推测该溶液为氯水(写名称).
0 158558 158566 158572 158576 158582 158584 158588 158594 158596 158602 158608 158612 158614 158618 158624 158626 158632 158636 158638 158642 158644 158648 158650 158652 158653 158654 158656 158657 158658 158660 158662 158666 158668 158672 158674 158678 158684 158686 158692 158696 158698 158702 158708 158714 158716 158722 158726 158728 158734 158738 158744 158752 203614
 某化学小组用以下装置做兴趣实验(试管中有空气存在).
某化学小组用以下装置做兴趣实验(试管中有空气存在).| 实验编号 | a中试剂 | b中试剂 |
| 1 | 0.1克Na、3mL水 | 0.1克Na、3mL乙醇 |
| 2 | 铁钉、3mL饱和食盐水 | 铁钉、3mL饱和氯化铵 |
| 3 | 3mL水 | 3mL饱和FeSO4溶液 |
| 4 | 3mL浓硝酸、1g铝片 | 3mL浓硝酸、1g铜片 |
a.左高右低b.左低右高c.左右相平d.来回震荡
(2)写出钠与乙醇反应的化学方程式2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;反应结束静置一段时间,最终U形管中液面c(填题(1)编号).
(3)实验2,U形管中液面a(填题(1)编号);写出a试管中发生还原反应的电极反应方程式O2+2H2O+4e→4OH-.
(4)实验3,U形管中液面左低右高,检验b管中生成新物质的操作是取样,加入KSCN溶液,溶液变红,说明有Fe3+生成.
(5)其他条件不变情况下,将实验4a、b试管中硝酸同时改为3mLcd(填编号),即可观察到U形管液面产生相反现象.
a.无水乙醇b.浓硫酸c.稀硫酸d.浓盐酸
(6)常温下,在a、b试管中分别加入等体积的同种溶液,仅对a试管进行强光照射,一段时间后观察到U型管液面左低右高,根据所学知识,推测该溶液为氯水(写名称).