4.中学化学教材中,常借助于图象的这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理.下列有关化学图象表现的内容正确的是( )
| A. | 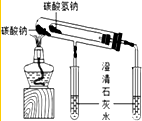 比较碳酸钠与碳酸氢钠的热稳定性 | B. |  称取NaOH | ||
| C. | 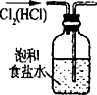 除去Cl2中HCl | D. | 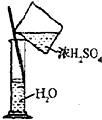 稀释浓H2SO4 |
3.在实验室中,对下列事故或药品的处理正确的是( )
| A. | 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | 蒸馏操作时,加热到较高温度时,发现未加沸石,应立即打开瓶塞加入沸石 | |
| D. | 含硫酸的废液倒入水槽,用水冲入下水道 |
2.氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
(1)BCl3的空间构型为;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生.
A. CsICl2═CsCl+ICl
B. CsICl2═CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是I.
(4)下列分子既不存在s-pσ键,也不存在p-pπ键的是D.
A. HCl B.HF C.CO2 D. SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3杂化,写出CN-的等电子体的分子式(写出1个)N2或CO.
(6)由H、N、O三种元素组成的常用作化肥,且水溶液显酸性化合物固态时属于离子晶体,假设其晶体的空间结构与氯化钠相似,且晶胞的棱长为acm,则该晶胞的密度为$\frac{320}{{N}_{A}•{a}^{3}}$g/cm3.
(1)BCl3的空间构型为;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生.
A. CsICl2═CsCl+ICl
B. CsICl2═CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是I.
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(KJ/mol) | 1681 | 1251 | 1140 | 1008 |
A. HCl B.HF C.CO2 D. SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3杂化,写出CN-的等电子体的分子式(写出1个)N2或CO.
(6)由H、N、O三种元素组成的常用作化肥,且水溶液显酸性化合物固态时属于离子晶体,假设其晶体的空间结构与氯化钠相似,且晶胞的棱长为acm,则该晶胞的密度为$\frac{320}{{N}_{A}•{a}^{3}}$g/cm3.
11.根据如图判断,下列说法正确的是( )
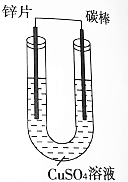

| A. | 该过程化学能转化为热能 | |
| B. | 该反应过程中只有化学键形成,没有化学键断裂 | |
| C. | CuSO4溶液里Cu2+移向负极 | |
| D. | 可以用铜片代替碳棒 |
9.下列关于相同质量的O2和臭氧(O3)的说法一定正确的是( )
| A. | 分子数之比为1:1 | B. | 原子数之比为1:1 | C. | 原子数之比为3:2 | D. | 物质的量之比2:3 |
8.将镁、铝各0.3mol分别放入100mL1mol•L-1的盐酸中,同温同压下产生气体的体积比是( )
0 158549 158557 158563 158567 158573 158575 158579 158585 158587 158593 158599 158603 158605 158609 158615 158617 158623 158627 158629 158633 158635 158639 158641 158643 158644 158645 158647 158648 158649 158651 158653 158657 158659 158663 158665 158669 158675 158677 158683 158687 158689 158693 158699 158705 158707 158713 158717 158719 158725 158729 158735 158743 203614
| A. | 2:3 | B. | 1:1 | C. | 3:2 | D. | 2:1 |
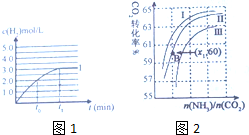 氨气是一种重要的化工产品,在生产和科研中应用广泛,氨气是工业合成氨的原料之一,工业上制取氨气有下列两种途径:
氨气是一种重要的化工产品,在生产和科研中应用广泛,氨气是工业合成氨的原料之一,工业上制取氨气有下列两种途径: