5.关于2mol SO2的叙述中,正确的是( )
| A. | 体积为44.8L | B. | 含有4mol氧原子 | ||
| C. | 分子数为6.02×1023 | D. | 摩尔质量为128g |
3.实验室常用氯化铵与氢氧化钙的固体混合物加热制取氨气,该反应的化学方程式为:2NH4Cl+Ca(OH)2$\stackrel{△}{→}$CaCl2+2NH3↑+2H2O.下列是实验室提供的有关装置:
(1)请从图中选择实验室制取氨气的气体发生装置b(填序号)、气体收集装置①(填序号).
(2)某学生用100mL注射器收集了50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后,注射器内无(填“有”或“无”)气体剩余,其中的液体呈红色,请用方程式解释液体颜色变化的原因:NH3+H2O?NH3•H2O?NH4++OH-.
(3)氨具有广泛的用途,它可用于制造化肥/制造硝酸/作冷却剂(举出一种即可).工业上合成氨常常要用铁触媒作催化剂,所加催化剂能否提高N2的转化率不能.理由是催化剂只改变化学反应速率,不影响平衡移动.
(4)工业合成氨的简易流程如下:

通过循环Ⅰ可利用的气态物质是D
A.催化剂 B.只有N2C.只有H2 D.N2和H2.
| 气体发生装置 | 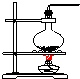 a |  b | 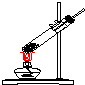 c |
| 气体收集装置 | 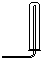 ① |  ② | 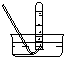 ③ |
(2)某学生用100mL注射器收集了50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后,注射器内无(填“有”或“无”)气体剩余,其中的液体呈红色,请用方程式解释液体颜色变化的原因:NH3+H2O?NH3•H2O?NH4++OH-.
(3)氨具有广泛的用途,它可用于制造化肥/制造硝酸/作冷却剂(举出一种即可).工业上合成氨常常要用铁触媒作催化剂,所加催化剂能否提高N2的转化率不能.理由是催化剂只改变化学反应速率,不影响平衡移动.
(4)工业合成氨的简易流程如下:

通过循环Ⅰ可利用的气态物质是D
A.催化剂 B.只有N2C.只有H2 D.N2和H2.
2.pH=3的醋酸与同体积的pH=11的NaOH溶液,混合后( )
| A. | 等于7 | B. | 小于7 | C. | 大于7 | D. | 不能确定 |
1.在25℃的纯水中,水的离子积(KW)为( )
| A. | KW=1×10-14 | B. | 大于1×10-14 | C. | 小于1×10-14 | D. | 0.01 |
20.二氧化硫转化为三氧化硫的过程中,加入催化剂的作用是( )
| A. | 能加大反应速率、促进平衡向三氧化硫的方向移动 | |
| B. | 能提高二氧化硫的利用率、使原料不被浪费 | |
| C. | 能提高三氧化硫的平衡浓度 | |
| D. | 加大正逆反应速率,缩短达到平衡的时间 |
19.下列关于阿佛加德罗常数(NA)的说法中不正确的是( )
0 158548 158556 158562 158566 158572 158574 158578 158584 158586 158592 158598 158602 158604 158608 158614 158616 158622 158626 158628 158632 158634 158638 158640 158642 158643 158644 158646 158647 158648 158650 158652 158656 158658 158662 158664 158668 158674 158676 158682 158686 158688 158692 158698 158704 158706 158712 158716 158718 158724 158728 158734 158742 203614
| A. | 1 mol N4分子的质量是56 g | |
| B. | 标况下,NA个 H2O分子含有3NA个原子 | |
| C. | 常温下,1 mo/L 的NH4Cl 溶液中NH4+的浓度小于1 mol/L | |
| D. | 高温高压,催化剂条件下,28 g N2分子与6 g H2充分反应可生成34 g NH3 |
 +H+=
+H+=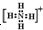 ;由5个原子核10个电子组成的化合物电子式是
;由5个原子核10个电子组成的化合物电子式是 ,结构式是
,结构式是 .
.