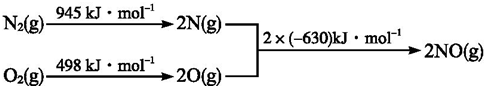
11.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L乙烷的分子数为NA | |
| B. | 1L0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 23g钠的原子最外层电子数为2NA | |
| D. | 1mol甲基所含质子数为10NA |
10.下列说法正确的是( )
| A. | 过滤、结晶、焰色反应、灼烧、萃取、分液和蒸馏等都是常用的分离混合物的方法 | |
| B. | 实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,然后涂上稀硼酸溶液 | |
| C. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| D. | 检验淀粉是否发生水解,可在溶液中滴加新制氢氧化铜悬浊液,加热至沸腾,若有红色沉淀生成说明已水解,反之则没有水解 |
9.在核反应方程24He+714N→817O+X中,X代表的粒子是( )
| A. | 11H | B. | 12H | C. | -10e | D. | 01n |
8.一定条件下,体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z.下列说法正确的是( )
| A. | 将容器体积变为20 L,Z的平衡浓度变为原来的1/2 | |
| B. | 以X的反应速率为0.001 mol•L-1•s-1 | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H>0 |
5.下列热化学方程式中,正确的是( )
| A. | 甲烷的燃烧热△H=-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 一定条件下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 在101 kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | HCl和NaOH反应的中和热△H,则相同温度下H2SO4和Ca(OH)2反应的热效应2△H |
2.H、C、N、O、Na、S、Cl是常见的七种短周期元素.
(1)N位于元素周期表第二 周期第ⅤA 族,其基态原子核外有3个未成对电子;S的基态原子核外电子排布式为1s22s22p63s23p4.
(2)用“>”或“<’’填空:
(3)由上述元素中的任意两种元素组成的化合物中,既含极性键又含非极性键的物质有H2O2、N2H4、C2H2、C2H4、C2H6、C6H6等任选其一(任写一种物质的分子式).
(4)NH3可作低温溶剂,它易液化的原因是NH3分子间能形成分子间氢键,氢键的存在使得氨气分子间作用力显著增强,沸点显著升高,易液化.已知25℃、101KPa,NH3能在纯氧中燃烧,每转移1mol e-,放出akJ热量,写出该条件下NH3燃烧的热化学方程式4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-4a kJ/mol.
(5)通常情况下,N2O5为无色晶体,它与Na2O2能发生反应(类似于CO2与Na2O2能反应),写出反应的化学方程式,并用单线桥标出电子转移的方向和数目: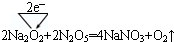 .
.
0 158509 158517 158523 158527 158533 158535 158539 158545 158547 158553 158559 158563 158565 158569 158575 158577 158583 158587 158589 158593 158595 158599 158601 158603 158604 158605 158607 158608 158609 158611 158613 158617 158619 158623 158625 158629 158635 158637 158643 158647 158649 158653 158659 158665 158667 158673 158677 158679 158685 158689 158695 158703 203614
(1)N位于元素周期表第二 周期第ⅤA 族,其基态原子核外有3个未成对电子;S的基态原子核外电子排布式为1s22s22p63s23p4.
(2)用“>”或“<’’填空:
| 第一电离能 | 电负性 | 稳定性 | 酸性 |
| N>O | C<N | H2S<H2O | H2SO4<HClO4 |
(4)NH3可作低温溶剂,它易液化的原因是NH3分子间能形成分子间氢键,氢键的存在使得氨气分子间作用力显著增强,沸点显著升高,易液化.已知25℃、101KPa,NH3能在纯氧中燃烧,每转移1mol e-,放出akJ热量,写出该条件下NH3燃烧的热化学方程式4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-4a kJ/mol.
(5)通常情况下,N2O5为无色晶体,它与Na2O2能发生反应(类似于CO2与Na2O2能反应),写出反应的化学方程式,并用单线桥标出电子转移的方向和数目:
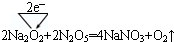 .
. 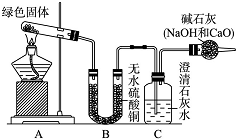 铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐.
铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐.