15.X、Y、Z、W是原子序数依次增大的短周期主族元素.Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4.下列说法正确的是( )
| A. | 原子半径:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Z的简单气态氢化物的热稳定性比Y的强 | |
| C. | 由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应 | |
| D. | 由X、Y、Z三种元素组成的化合物可以是酸、碱或盐 |
14.对SO2与CO2说法正确的是( )
| A. | 都是极性分子 | B. | 中心原子都采取sp杂化 | ||
| C. | SO2为V形结构,CO2为直线形结构 | D. | S原子和C原子上都没有孤电子对 |
13.下列各组元素性质递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | N、O、F元素最高正化合价依次升高 | |
| C. | P、S、Cl原子半径依次增大 | |
| D. | Na、K、Rb的第一电离能依次减小 |
12.已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A. | X与Y形成的化合物中,X可以显负价,Y显正价 | |
| B. | 最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性 | |
| C. | 第一电离能X一定大于Y | |
| D. | 气态氢化物的稳定性:HmY小于HnX |
11.关于碱金属单质的性质叙述错误的是( )
| A. | 钠在空气中燃烧的生成物是过氧化钠 | |
| B. | 与水反应时都能生成碱和氢气 | |
| C. | 熔沸点随原子序数增加而升高 | |
| D. | 碱金属单质还原性随原子电子层数的增加而增加 |
10.已知NCl3的熔点为-40°C,沸点为71℃.下列叙述正确的是( )
| A. | NCl3属于离子晶体 | B. | NCl3中心氮原子为sp2杂化 | ||
| C. | NCl3空间构型为平面三角形 | D. | NCl3分子属于极性分子 |
9.下列各原子或离子的基态电子排布式错误的是( )
| A. | Al 1s22s22p63s13p2 | B. | Cl- 1s22s22p63s23p6 | ||
| C. | Na+ 1s22s22p6 | D. | F 1s22s22p5 |
8.下列化合物中,既有离子键,又有共价键且是非极性共价键的是( )
| A. | NaOH | B. | Na2O2 | C. | H2O2 | D. | NH4Cl |
7.下列化学用语说法正确的是( )
0 158498 158506 158512 158516 158522 158524 158528 158534 158536 158542 158548 158552 158554 158558 158564 158566 158572 158576 158578 158582 158584 158588 158590 158592 158593 158594 158596 158597 158598 158600 158602 158606 158608 158612 158614 158618 158624 158626 158632 158636 158638 158642 158648 158654 158656 158662 158666 158668 158674 158678 158684 158692 203614
| A. | 氮原子电子排布图为: | |
| B. | S2-的结构示意图: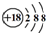 | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| D. | 氯化钠的电子式: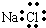 |
 ClO2是一种国际上公认的安全无毒的绿色水处理剂.回答下列问题:
ClO2是一种国际上公认的安全无毒的绿色水处理剂.回答下列问题: