16.以下有关NO2气体的描述中正确的是( )
| A. | 据反应3NO2+H2O═2HNO3+NO可知,NO2是HNO3的酸酐 | |
| B. | 据反应2NO2(g)?N2O4(g)△<0可知要制得较纯净的NO2,需高温、低压环境 | |
| C. | 据反应Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O和3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,可知浓HNO3的氧化性不如稀HNO3强 | |
| D. | NO2、Br2(g)同为红棕色气体,可用湿润的淀粉-KI试纸鉴别 |
15.某化妆品的组分Z具有美白功效,原从杨树中提取,12.现可用如下反应制备,下列叙述错误的是( )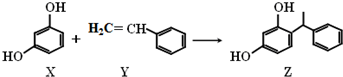

| A. | X、Y和Z均能与溴水发生反应,其中X、Z发生取代反应,Y发生加成反应 | |
| B. | X和Z均能NaOH溶液反应,也能与NaHCO3溶液反应放出CO2 | |
| C. | Y既能与H2发生加成反应,也能使酸性高锰酸钾溶液褪色 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
14.下列化学用语表达正确的是( )
| A. | 对硝基甲苯的结构简式: | B. | S2-离子的结构示意图: | ||
| C. | CO2的分子比例模型: | D. | 次氯酸的电子式: |
12.已知氧化性Br2>Fe3+.FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:
a Fe2++b Br-+c Cl2→d Fe3++e Br2+f Cl-
下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
0 158482 158490 158496 158500 158506 158508 158512 158518 158520 158526 158532 158536 158538 158542 158548 158550 158556 158560 158562 158566 158568 158572 158574 158576 158577 158578 158580 158581 158582 158584 158586 158590 158592 158596 158598 158602 158608 158610 158616 158620 158622 158626 158632 158638 158640 158646 158650 158652 158658 158662 158668 158676 203614
a Fe2++b Br-+c Cl2→d Fe3++e Br2+f Cl-
下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
 铬元素及其化合物在生产、生活中具有广泛的用途.
铬元素及其化合物在生产、生活中具有广泛的用途.