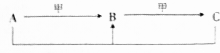
6.表是周期表中的一部分,根据A-I的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne.
(2)A-I元素中,非金属性最强的元素与金属性最强的元素形成的物质是Na,该物质的熔点比干冰的熔点高(填“低”或“高”).
(3)比较D、E最高价氧化物的水化物酸性强弱HNO3>H2CO3.
(4)G、H的氢化物沸点较高的是HF,理由是HF分子间含氢键.
(5)A、E、H组成的常见物质的电子式为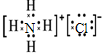 .
.
(6)用电子式表示E的氢化物的形成过程3H•+ →
→ .
.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | F | G | I | |||
| 3 | B | C | H |
(2)A-I元素中,非金属性最强的元素与金属性最强的元素形成的物质是Na,该物质的熔点比干冰的熔点高(填“低”或“高”).
(3)比较D、E最高价氧化物的水化物酸性强弱HNO3>H2CO3.
(4)G、H的氢化物沸点较高的是HF,理由是HF分子间含氢键.
(5)A、E、H组成的常见物质的电子式为
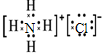 .
.(6)用电子式表示E的氢化物的形成过程3H•+
 →
→ .
.
5.下列各组原子中,彼此化学性质一定相似的是( )
| A. | 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 | |
| B. | 2p轨道上只有一个成单电子的X原子与3p轨道上只有一个成单电子的Y原子 | |
| C. | 2p轨道上有一个空轨道的X原子与3p轨道上有一个空轨道的Y原子 | |
| D. | 最外层都只有1个电子的X、Y原子 |
4.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 12g的金刚石晶体中含有碳碳键的数目为4NA | |
| B. | 4g氦气含有的原子总数为NA | |
| C. | 石墨中C和C-C键的比为2:3 | |
| D. | 60gSiO2含有Si-O键的个数为2NA |
3.下列表达方式正确的是( )
| A. | CO2的分子模型示意图: | |
| B. | 硫原子的轨道表示式为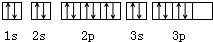 | |
| C. | 硫离子的核外电子排布式 1s22s22p63s23p4 | |
| D. | 碳-12原子构成 ${\;}_{6}^{12}$C |
2.下列各组物质的晶体,化学键类型相同,晶体类型也相同的是( )
| A. | SO2和SiO2 | B. | NaOH和NaCl | C. | NH4Cl 和HCl | D. | H2O2和C3H6 |
1.下列关于弱电解质的电离平衡常数的叙述中,正确的是( )
0 158480 158488 158494 158498 158504 158506 158510 158516 158518 158524 158530 158534 158536 158540 158546 158548 158554 158558 158560 158564 158566 158570 158572 158574 158575 158576 158578 158579 158580 158582 158584 158588 158590 158594 158596 158600 158606 158608 158614 158618 158620 158624 158630 158636 158638 158644 158648 158650 158656 158660 158666 158674 203614
| A. | 因为电离过程是吸热过程,所以温度越高,同一弱电解质的电离平衡常数越大,电离度越小 | |
| B. | 弱电解质的电离平衡常数是由各微粒的平衡浓度表达的,所以弱电解质的电离平衡常数只与浓度有关 | |
| C. | 对于不同的弱酸,电离平衡常数越大,酸性一定越强,可以通过电离平衡常数的大小判断弱酸的相对强弱 | |
| D. | 弱电解质的电离平衡常数是衡量弱电解质电离程度大小的一种方法 |