1.将Na2O2投入FeCl3溶液中,可观察到的现象是( )
| A. | 生成白色沉淀 | B. | 有气泡产生,生成红褐色沉淀 | ||
| C. | 有气泡产生 | D. | 无变化 |
20.下列各组物质之间不可能实现如图所示转化的是( )


| 选项 | X | Y | Z | M |
| A | O2 | CO2 | CO | C |
| B | CH3CH2OH | CH3CHO | CH3COOH | O2 |
| C | NaOH | NaHCO3 | Na2CO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A. | A | B. | B | C. | C | D. | D |
19.密度为0.910g/cm3酒精水溶液,质量分数为25.0%,该酒精水溶液用等体积的水稀释后,所得溶液的质量分数为( )
| A. | 等于13.5% | B. | 大于12.5% | C. | 小于12.5% | D. | 无法确定 |
16.已知浓硫酸和木炭粉在加热条件下可发生化学反应.
(1)上述反应的化学方程式为2H2SO4(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O.
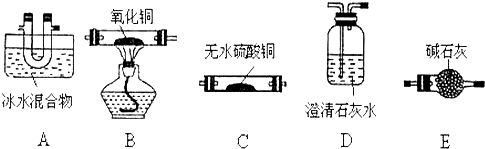
(2)试用如图所列各装置设计一个实验,来验证上述反应所产生的各种产物.
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置中导管口的编号):
g接c,d接a,b接f.
(3)实验时可观察到装置①中A瓶中的溶液褪色,C瓶中的溶液不褪色.A瓶中的溶液的作用是检验SO2气体;B瓶中的溶液的作用是吸收SO2气体;C瓶中的溶液的作用是检验SO2气体是否除干净.
(4)装置②中所加固体药品是无水硫酸铜.可验证的产物是H2O.
(5)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.
(1)上述反应的化学方程式为2H2SO4(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O.
(2)试用如图所列各装置设计一个实验,来验证上述反应所产生的各种产物.
| 编号 | ① | ② | ③ | ④ |
| 装置 |  |  |  |  |
g接c,d接a,b接f.
(3)实验时可观察到装置①中A瓶中的溶液褪色,C瓶中的溶液不褪色.A瓶中的溶液的作用是检验SO2气体;B瓶中的溶液的作用是吸收SO2气体;C瓶中的溶液的作用是检验SO2气体是否除干净.
(4)装置②中所加固体药品是无水硫酸铜.可验证的产物是H2O.
(5)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.
14.工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)获取铜和胆矾的操作流程如下:

已知:①部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)已知Cu2O在酸性条件下发生自身氧化还原反应,写出离子反应方程式Cu2O+2H+=Cu+Cu2++H2O.
(2)为了加快反应Ⅰ的速率,可以采取的措施是升高温度、不断搅拌、将矿渣粉碎、增大硫酸的浓度(写2点).
(3)固体混合物A中的成分是SiO2、Cu.
(4)反应Ⅰ完成后,铁元素的存在形式为Fe2+(填离子符号);写出生成该离子的离子方程式2Fe3++Cu=Cu2++2Fe2+.
(5)x对应的数值范围是3.2≤pH<4.0.
(6)用NaClO调pH,生成沉淀B的反应的离子方程式为2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+.
(7)洗涤CuSO4•5H2O粗产品不能用大量水洗,而用冰水洗涤,原因是CuSO4可溶于水,冰水可以减少CuSO4晶体的损失.
0 158439 158447 158453 158457 158463 158465 158469 158475 158477 158483 158489 158493 158495 158499 158505 158507 158513 158517 158519 158523 158525 158529 158531 158533 158534 158535 158537 158538 158539 158541 158543 158547 158549 158553 158555 158559 158565 158567 158573 158577 158579 158583 158589 158595 158597 158603 158607 158609 158615 158619 158625 158633 203614

已知:①部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(2)为了加快反应Ⅰ的速率,可以采取的措施是升高温度、不断搅拌、将矿渣粉碎、增大硫酸的浓度(写2点).
(3)固体混合物A中的成分是SiO2、Cu.
(4)反应Ⅰ完成后,铁元素的存在形式为Fe2+(填离子符号);写出生成该离子的离子方程式2Fe3++Cu=Cu2++2Fe2+.
(5)x对应的数值范围是3.2≤pH<4.0.
(6)用NaClO调pH,生成沉淀B的反应的离子方程式为2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+.
(7)洗涤CuSO4•5H2O粗产品不能用大量水洗,而用冰水洗涤,原因是CuSO4可溶于水,冰水可以减少CuSO4晶体的损失.