11. 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
(1)Y原子核外共有7种不同运动状态的电子,基态T原子有7种不同能级的电子.
(2)X、Y、Z的第一电离能由小到大的顺序为C<O<N(用元素符号表示).
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为sp杂化.
(4)Z与R能形成化合物甲,1mol甲中含4 mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为SiF4为正四面体形、H2O为V形.
(5)G、Q、R氟化物的熔点如表,造成熔点差异的原因为NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小、电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高.
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
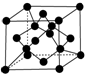
(7)X单质的晶胞如图所示,一个X晶胞中有8个X原子;若X晶体的密度为ρ g•cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个X原子之间的距离为$\frac{\sqrt{3}}{4}×\root{3}{\frac{96}{ρ{N}_{A}}}$ cm(用代数式表示).
 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.(1)Y原子核外共有7种不同运动状态的电子,基态T原子有7种不同能级的电子.
(2)X、Y、Z的第一电离能由小到大的顺序为C<O<N(用元素符号表示).
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为sp杂化.
(4)Z与R能形成化合物甲,1mol甲中含4 mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为SiF4为正四面体形、H2O为V形.
(5)G、Q、R氟化物的熔点如表,造成熔点差异的原因为NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低;Mg2+的半径比Na+的半径小、电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高.
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1 539 | 183 |
(7)X单质的晶胞如图所示,一个X晶胞中有8个X原子;若X晶体的密度为ρ g•cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个X原子之间的距离为$\frac{\sqrt{3}}{4}×\root{3}{\frac{96}{ρ{N}_{A}}}$ cm(用代数式表示).
8. 下表给出五种元素的相关信息,根据以下信息填空:
下表给出五种元素的相关信息,根据以下信息填空:
(1)元素Y基态原子的核外电子排布式为1s22s22p63s23p64s2(或[Ar]4s2).
(2)42gT的单质分子中π键的个数为3NA;在T的最简单氢化物分子中T原子的杂化类型是sp3.研究者预想合成一个纯粹由T元素组成的新物种T5+T3-,若T5+离子中每个氮原子均满足8电子且呈对称结构,以下有关T5+推测正确的是BD(填序号)
A.N5+有24个电子
B.N5+阳离子中存在两个氮氮三键
C.N5+离子中存在三对未成键的电子对
D.N3-离子的空间构型为直线型
(3)TX3是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用.它可在Z单质的催化作用下由X2和过量的TH3反应得到,试写出该反应的化学方程式:4NH3+3F2$\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F.在该反应方程式中的几种物质所属的晶体类型有acd(填序号).
a.离子晶体 b.原子晶体 c.分子晶体 d.金属晶体
(4)T、W、X 3种元素的电负性由大到小的顺序为F>O>N(用元素符号表示).
(5)Z2+能与T的氢化物写出配位数为4的配离子[Z(TH3)4]2+,该配离子具有对称的空间构型,且离子中的两个TH3被两个Cl取代只能得到一种产物,则[Z(TH3)4]2+的空间构型为正四面体.
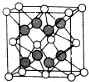
(6)X和Y形成的化合物的晶胞结构如图所示,已知晶体的密度为ρ g•cm-3,阿伏加德罗常数为NA,则晶胞边长a=$\root{3}{\frac{312ρ}{{N}_{A}}}$cm.(用ρ、NA的计算式表示).
 下表给出五种元素的相关信息,根据以下信息填空:
下表给出五种元素的相关信息,根据以下信息填空:| 元素 | 相关信息 |
| T | 基态原子2p能级有3个单电子 |
| W | 基态原子p轨道上成对电子数等于未成对电子数 |
| X | 氢化物常用于刻蚀玻璃 |
| Y | 基态原子核外电子分处6个不同能级,且每个能级均已排满 |
| Z | 原子序数等于X与Y的原子序数之和 |
(2)42gT的单质分子中π键的个数为3NA;在T的最简单氢化物分子中T原子的杂化类型是sp3.研究者预想合成一个纯粹由T元素组成的新物种T5+T3-,若T5+离子中每个氮原子均满足8电子且呈对称结构,以下有关T5+推测正确的是BD(填序号)
A.N5+有24个电子
B.N5+阳离子中存在两个氮氮三键
C.N5+离子中存在三对未成键的电子对
D.N3-离子的空间构型为直线型
(3)TX3是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用.它可在Z单质的催化作用下由X2和过量的TH3反应得到,试写出该反应的化学方程式:4NH3+3F2$\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F.在该反应方程式中的几种物质所属的晶体类型有acd(填序号).
a.离子晶体 b.原子晶体 c.分子晶体 d.金属晶体
(4)T、W、X 3种元素的电负性由大到小的顺序为F>O>N(用元素符号表示).
(5)Z2+能与T的氢化物写出配位数为4的配离子[Z(TH3)4]2+,该配离子具有对称的空间构型,且离子中的两个TH3被两个Cl取代只能得到一种产物,则[Z(TH3)4]2+的空间构型为正四面体.
(6)X和Y形成的化合物的晶胞结构如图所示,已知晶体的密度为ρ g•cm-3,阿伏加德罗常数为NA,则晶胞边长a=$\root{3}{\frac{312ρ}{{N}_{A}}}$cm.(用ρ、NA的计算式表示).
3.工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如图1:

已知部分物质沉淀的pH及CaSO4的溶解度曲线如图2:
(1)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH到约3.2,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除尽;
②将浊液加热到 80℃,趁热过滤
(2)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+,
(3)当离子浓度小于或等于1×10-5 mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥4.0×10-9mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].
0 158432 158440 158446 158450 158456 158458 158462 158468 158470 158476 158482 158486 158488 158492 158498 158500 158506 158510 158512 158516 158518 158522 158524 158526 158527 158528 158530 158531 158532 158534 158536 158540 158542 158546 158548 158552 158558 158560 158566 158570 158572 158576 158582 158588 158590 158596 158600 158602 158608 158612 158618 158626 203614

已知部分物质沉淀的pH及CaSO4的溶解度曲线如图2:
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
①加入石灰乳调节pH到约3.2,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除尽;
②将浊液加热到 80℃,趁热过滤
(2)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+,
(3)当离子浓度小于或等于1×10-5 mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥4.0×10-9mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].
 A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:
A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:


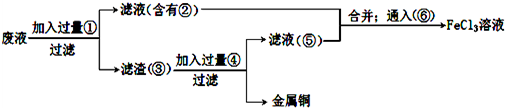
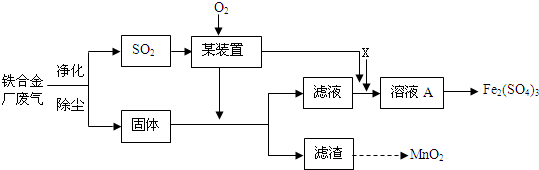

 .该工艺设计中,过量X参与反应的离子方程式是:AlO2-+CO2+2H2O=Al(OH)3+HCO3-.
.该工艺设计中,过量X参与反应的离子方程式是:AlO2-+CO2+2H2O=Al(OH)3+HCO3-.