8.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 苏打和氢氧化铝胶囊,可以作内服药治疗胃酸过多 | |
| C. | Al2O3和MgO的熔点均很高,可用于制作耐高温材料 | |
| D. | NaHCO3可用作发酵粉、泡沫灭火剂材料、治疗胃酸过多的药物 |
7.在如图所示的装置中,a的金属活泼性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
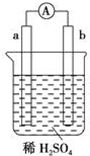

| A. | 碳棒上有气体放出,溶液pH变大 | |
| B. | a是正极,b是负极 | |
| C. | 稀硫酸中有电子流动,方向是从b极到a极 | |
| D. | a极上发生了氧化反应 |
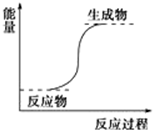
6.下列反应一定属于放热反应的是( )

| A. | 氢氧化钡晶体和氯化铵晶体的反应 | |
| B. | 能量变化如图所示的反应 | |
| C. | 化学键断裂吸收的能量比化学键形成放出的能量少的反应 | |
| D. | 不需要加热就能发生的反应 |
3.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 LCH4中含有氢原子数目为4NA | |
| B. | 1 molNa2O2中含有的阴离子和阳离子的数目为2NA | |
| C. | 0.1 mol/LCu(NO3)2溶液中含有的离子数目为0.2NA | |
| D. | 28 gN2中所含的原子数目为NA |
2.从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分:
甲: 乙:
乙:
丙:
请回答下列问题:
(1)甲中含氧官能团的名称为羟基.
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

其中反应Ⅰ的类型为加成反应,反应Ⅱ的化学方程式为 (注明反应条件).
(注明反应条件).
(3)已知:RCH=CHR'$→_{ii.Zn/H_{2}O}^{i.O_{3}}$RCHO+R'CHO;2HCHO$\underset{\stackrel{i.浓NaOH}{→}}{ii.{H}^{+}}$HCOOH+CH3OH.
由乙制丙的一种合成路线如图所示(A~F均为有机物,图中Mr表示相对分子质量):

①下列物质不能与C反应的是c(填序号).
a.金属钠 b.HBr c.Na2CO3溶液 d.乙酸
②E的结构结构简式:HOCH2COOH
③写出反应方程式C+D→丙: +
+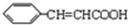 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$  +H2O
+H2O
④D有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体的结构简式 .
.
a.苯环上连接三种不同的官能团 b.能发生银镜反应
c.能与Br2/CCl4发生加成反应 d.遇FeCl3溶液显示特征颜色.
甲:
 乙:
乙:
丙:
| 分子式 | C16H14O2 |
| 部分性质 | 能使Br2/CCl4褪色 |
| 能在稀硫酸中水解 |
(1)甲中含氧官能团的名称为羟基.
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

其中反应Ⅰ的类型为加成反应,反应Ⅱ的化学方程式为
 (注明反应条件).
(注明反应条件).(3)已知:RCH=CHR'$→_{ii.Zn/H_{2}O}^{i.O_{3}}$RCHO+R'CHO;2HCHO$\underset{\stackrel{i.浓NaOH}{→}}{ii.{H}^{+}}$HCOOH+CH3OH.
由乙制丙的一种合成路线如图所示(A~F均为有机物,图中Mr表示相对分子质量):

①下列物质不能与C反应的是c(填序号).
a.金属钠 b.HBr c.Na2CO3溶液 d.乙酸
②E的结构结构简式:HOCH2COOH
③写出反应方程式C+D→丙:
 +
+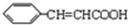 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$  +H2O
+H2O④D有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体的结构简式
 .
.a.苯环上连接三种不同的官能团 b.能发生银镜反应
c.能与Br2/CCl4发生加成反应 d.遇FeCl3溶液显示特征颜色.
1.现有含FeCl2杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按下图所示步骤进行提纯:
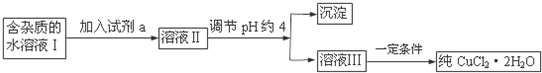
25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
请回答下列问题:
(1)流程中加入的试剂a最合适的是C(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是将Fe2+氧化.
(2)调节pH约4应该加入的物质可以是AC.
A.CuO B.CuCl2C.Cu(OH)2D.NaOH
(3)最后能不能直接蒸发结晶得到CuCl2•2H2O?不能(填“能”或“不能”).理由:加热促进铜离子水解,生成的HCl易挥发,则不能直接蒸发结晶得到CuCl2•2H2O.

25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 4.7 |
| 完成沉淀pH | 3.2 | 9.7 | 6.7 |
(1)流程中加入的试剂a最合适的是C(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是将Fe2+氧化.
(2)调节pH约4应该加入的物质可以是AC.
A.CuO B.CuCl2C.Cu(OH)2D.NaOH
(3)最后能不能直接蒸发结晶得到CuCl2•2H2O?不能(填“能”或“不能”).理由:加热促进铜离子水解,生成的HCl易挥发,则不能直接蒸发结晶得到CuCl2•2H2O.
20.表是不同温度下水的离子积常数:
试回答以下问题:
T2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=9:11.此溶液中各种离子的浓度由大到小的顺序是c(Na+)>c(SO42-)>c(H+)>c(OH-).
0 158409 158417 158423 158427 158433 158435 158439 158445 158447 158453 158459 158463 158465 158469 158475 158477 158483 158487 158489 158493 158495 158499 158501 158503 158504 158505 158507 158508 158509 158511 158513 158517 158519 158523 158525 158529 158535 158537 158543 158547 158549 158553 158559 158565 158567 158573 158577 158579 158585 158589 158595 158603 203614
| 温度/℃ | 25 | T2 |
| 水的离子积常数 | 1×10-14 | 1×10-12 |
T2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=9:11.此溶液中各种离子的浓度由大到小的顺序是c(Na+)>c(SO42-)>c(H+)>c(OH-).