9.下列有机化合物中,既能与盐酸起反应,又能与NaOH溶液反应的是( )
| A. | 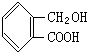 | B. | 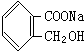 | C. | H2NCH2COONa | D. | H2NCH2COOH |
8.某无色透明溶液中,由水电离出来的[H+]=1×10-11 mol•L-1,该溶液中一定能大量共存离子组是( )
| A. | K+、Na+、MnO4-、NO3- | B. | K+、Na+、Cl-、NO3- | ||
| C. | NH4+、AlO2-、Na+、CH3COO- | D. | Fe3+、S2-、Al3+、HCO3- |
7.下列叙述正确的是( )
| A. | 同主族金属的原子半径越大熔点越高 | |
| B. | 稀有气体原子序数越大沸点越高 | |
| C. | 同周期元素的原子半径越小越易失去电子 | |
| D. | 在晶体中只要有阳离子就一定有阴离子 |
5.传统饮用水的消毒剂是氯气.二十世纪八十年代初期科研人员在英国某城调查发现,儿童患白血病发病率高是源于饮用了氯气消毒的饮用水,这是因为( )
| A. | 氯气有氧化性,作用于正常细胞而癌化 | |
| B. | 氯水中的次氯酸具有杀菌性,氧化了正常细胞,异化为癌细胞 | |
| C. | 氯气有毒,杀死正常细胞,不杀灭癌细胞 | |
| D. | 氯气作用于水中有机物,生成有机氯化合物而致癌 |
4.室温下,有两种溶液:①0.01mol•L-1 NH3•H2O 溶液、②0.01mol•L-1 NH4Cl 溶液,下列操作可以使两种溶液中 c(NH4+)都增大的是( )
| A. | 通入少量 HCl 气体 | B. | 加入少量 NaOH 固体 | ||
| C. | 加入少量 H2O | D. | 适当升高温度 |
2.对于某些离子的检验方法(包括操作、现象、结论),完全正确的是( )
| A. | 向待测溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 向待测溶液中逐滴加入氢氧化钠溶液,开始有白色沉淀生成,继续滴加氢氧化钠溶液到过量,沉淀逐渐溶解,一定有 Al3+ | |
| C. | 向待测溶液中先滴加盐酸酸化未出现沉淀,再加入 BaCl2 溶液有白色沉淀产生,一定有SO42- | |
| D. | 向待测溶液中滴加 NaOH 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,一定有NH4+ |
1. 某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
(1)现有以下仪器和用品:橡胶管、秒表、温度计、a mol/L 稀硝酸、b mol/L 稀硝酸及图中仪器.
①写出本实验的化学方程式:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,并标出电子转方向和数目: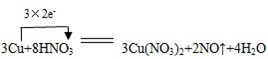 .
.
②设计实验方案:在相同稀硝酸浓度、不同温度(或相同温度、不同稀硝酸浓度下,测定相同时间内产生气体体积(或产生相同体积的气体所需的时间).
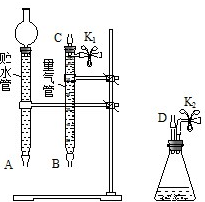
③在如图中将 A、B、C、D、几处用橡胶管以正确方式连接起来,以测定反应所产生气体的体积(三个容器中的液体和水都已出).
④测定前,为避免 NO 被氧化为 NO2,要用 CO2排出锥形瓶和橡胶管中的空气:在锥形瓶中加入铜片后松开 K2弹簧夹,从 K2处的橡胶管向装置中通入 CO2,此时 K1处应进行的操作是松开K1弹簧夹,接导管通入澄清石灰水至出现白色浑浊为止,则空气已排尽.
(2)注入稀硝酸后,在给定条件下设计实验探究浓度和温度对化学反应速率的影响:温度25℃、50℃;时间 t1、t2、t3;收集气体体积 V1、V2.请完成表:
 某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.(1)现有以下仪器和用品:橡胶管、秒表、温度计、a mol/L 稀硝酸、b mol/L 稀硝酸及图中仪器.
①写出本实验的化学方程式:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,并标出电子转方向和数目:
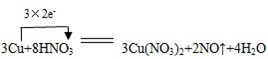 .
.②设计实验方案:在相同稀硝酸浓度、不同温度(或相同温度、不同稀硝酸浓度下,测定相同时间内产生气体体积(或产生相同体积的气体所需的时间).
③在如图中将 A、B、C、D、几处用橡胶管以正确方式连接起来,以测定反应所产生气体的体积(三个容器中的液体和水都已出).
④测定前,为避免 NO 被氧化为 NO2,要用 CO2排出锥形瓶和橡胶管中的空气:在锥形瓶中加入铜片后松开 K2弹簧夹,从 K2处的橡胶管向装置中通入 CO2,此时 K1处应进行的操作是松开K1弹簧夹,接导管通入澄清石灰水至出现白色浑浊为止,则空气已排尽.
(2)注入稀硝酸后,在给定条件下设计实验探究浓度和温度对化学反应速率的影响:温度25℃、50℃;时间 t1、t2、t3;收集气体体积 V1、V2.请完成表:
| 实验编号 | 稀硝酸的浓度 /(mol/L) | 稀硝酸的体积 /mL | 温度 /℃ | 时间 /min | 收集气体的体积/mL |
| ① | a | V | 25 | t1 | V1 |
| ② | V | ||||
| ③ | V |
20.阅读如表中的部分短周期主族元素的相关信息
请回答下列问题:
(1)描述 Z 元素在周期表中的位置第三周期第ⅦA 族:
(2)T、X、Y 元素简单离子半径由大到小的顺序为:O2->Na+>Al3+(填离子符号)
(3)已知 1mol 化合物 A 与 Na2SO3在溶液中发生反应时,转移 2mol 电子,写出该反应的离子方程式ClO-+SO32-=Cl-+SO42-.
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是随着原子序数的递增,E 值增大.
②根据如图提供的信息,试推断E氟>E氧(填“>”“<”或“=”).
0 158397 158405 158411 158415 158421 158423 158427 158433 158435 158441 158447 158451 158453 158457 158463 158465 158471 158475 158477 158481 158483 158487 158489 158491 158492 158493 158495 158496 158497 158499 158501 158505 158507 158511 158513 158517 158523 158525 158531 158535 158537 158541 158547 158553 158555 158561 158565 158567 158573 158577 158583 158591 203614
| 元素代号 | 相关信息 |
| T | T 的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X 的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期金属元素中,Y 的简单离子半径最小 |
| Z | T、X、Z 组成的 36 电子的化合物 A 是家用消毒剂的主要成分 |
(1)描述 Z 元素在周期表中的位置第三周期第ⅦA 族:
(2)T、X、Y 元素简单离子半径由大到小的顺序为:O2->Na+>Al3+(填离子符号)
(3)已知 1mol 化合物 A 与 Na2SO3在溶液中发生反应时,转移 2mol 电子,写出该反应的离子方程式ClO-+SO32-=Cl-+SO42-.
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是随着原子序数的递增,E 值增大.
②根据如图提供的信息,试推断E氟>E氧(填“>”“<”或“=”).
 甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和.甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M.
甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和.甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M.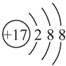 .
.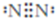 .
.