5.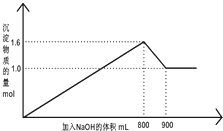 向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:
向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:
(1)加入NaOH 溶液900mL 时,溶液中的沉淀是Fe(OH)3,溶液中的溶质是NaCl、NaAlO2.(填化学式)
(2)加入NaOH 溶液800mL 至900mL 之间时,发生的离子反应方程式是Al(OH)3+OH-=AlO2-+2H2O
(3)将混合溶液中各溶质的物质的量浓度填入下表:
(4)加入NaOH 的溶液物质的量浓度为8mol/L.
 向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:
向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:(1)加入NaOH 溶液900mL 时,溶液中的沉淀是Fe(OH)3,溶液中的溶质是NaCl、NaAlO2.(填化学式)
(2)加入NaOH 溶液800mL 至900mL 之间时,发生的离子反应方程式是Al(OH)3+OH-=AlO2-+2H2O
(3)将混合溶液中各溶质的物质的量浓度填入下表:
| 溶质 | A1Cl3 | FeCl3 |
| 物质的量浓度 mol/L |
4.观察下列模型并结合相关信息,判断下列说法中不正确的是( )
| B12结构单元 | SF6 | S8 | HCN |
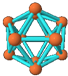 | 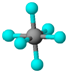 | 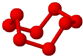 | 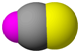 |
| 熔点1873K | 气体 | 易溶于CS2 | 溶液显弱酸性 |
| A. | 单质B12形成的晶体可能为原子晶体 | |
| B. | SF6是由极性键构成的非极性分子 | |
| C. | S8和HCN形成晶体后,晶体类型相同 | |
| D. | HCN形成晶体后,晶体中的作用力只有共价键 |
3.NaF、NaI、MgO晶体均为离子晶体,根据下列数据,这三种晶体的熔点高低顺序是( )
| 物质 | NaF | NaI | MgO |
| 离子所带电荷数 | 1 | 1 | 2 |
| 离子核间距离/10-10m | 2.31 | 3.18 | 2.10 |
| A. | NaF>NaI>MgO | B. | MgO>NaF>NaI | C. | MgO>NaI>NaF | D. | NaI>NaF>MgO |
2.下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是( )
| A. | MgO和SiC | B. | Fe和S | C. | CO2 和SiO2 | D. | 碘和干冰升华 |
1.下列式子为分子式的是( )
| A. | NH4Cl | B. | Cu | C. | SiO2 | D. | I2 |
20.肼(N2H4)能与硫酸反应生成N2H6SO4,已知N2H6SO4的晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在( )
0 158391 158399 158405 158409 158415 158417 158421 158427 158429 158435 158441 158445 158447 158451 158457 158459 158465 158469 158471 158475 158477 158481 158483 158485 158486 158487 158489 158490 158491 158493 158495 158499 158501 158505 158507 158511 158517 158519 158525 158529 158531 158535 158541 158547 158549 158555 158559 158561 158567 158571 158577 158585 203614
| A. | 离子键 | B. | 共价键 | C. | 配位键 | D. | 范德华力 |