19.下列叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都发生失电子的氧化反应 | |
| B. | 原电池是自发的氧化还原反应,电解池发生的是不自发的氧化还原发应 | |
| C. | 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量大 | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
18.把1L含乙烯和H2的混合气体通过Ni催化剂,使乙烯和H2发生加成反应,完全反应后,气体体积变为yL(气体体积均在同温、同压下测定).若乙烯在1L混合气体中的体积分数为a%,则a%和y的关系一定不正确的是( )
| A. | y=1×a% | B. | y=1-1×a% | C. | y=1×a%=0.5 | D. | y=1-1×a%<0.5 |
17.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 50ml盐酸 | 50ml盐酸 | 50ml盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A. | 15.7g混合物能恰好与盐酸完全反应 | |
| B. | 根据表中数据不能计算出混合物中NaHCO3的质量分数 | |
| C. | 向50ml盐酸中加入混合物27.6g时,盐酸过量 | |
| D. | 盐酸的物质的量浓度为3.0mol/L |
16.下列反应既是氧化还原,又是吸热反应的是( )
| A. | 镁条与稀H2SO4反应 | |
| B. | 乙醇在氧气中的燃烧反应 | |
| C. | Ba(OH)2•8H2O与NH4Cl | |
| D. | 炽热的焦炭和水蒸气反应制取水煤气 |
15.下列对应的表达方式错误的是( )
| A. | Cl-的结构示意图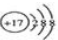 | B. | 氯化氢分子的电子式: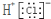 | ||
| C. | 碳-12原子${\;}_{5}^{12}C$ | D. | HClO的结构式H-O-Cl |
14.下列关于节能与可再生能源表述不正确的是( )
| A. | “低碳”意指更低的二氧化碳气体的排放 | |
| B. | 太阳能、水能、风能都属于可再生能源 | |
| C. | 太阳能电池的工作原理是光能与化学能的转换 | |
| D. | 利用燃气轮机进行天然气发电不属于可再生能源利用 |
13.SiCl4的分子结构与CCl4类似,对其作出如下推断:①SiCl4是正四面体构型:②常温常压下SiCl4是液体;③SiCl4的分子是由极性键形成的分子;④SiCl4熔点高于CCl4.其中正确的是( )
| A. | 只有① | B. | 只有①② | C. | 只有②③ | D. | ①②③④ |
12.氢气还原氧化铜:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,该反应中( )
| A. | H2作氧化剂 | B. | 铜元素化合价升高 | ||
| C. | 氢元素化合价降低 | D. | Cu是还原产物 |
11.下列氯化物中不能用金属和氯气直接反应制得的是( )
| A. | CuCl2 | B. | FeCl2 | C. | FeCl3 | D. | NaCl |
10.某化学兴趣小组利用如图装置进行乙酸乙酯合成和分离的实验探究,请回答以下问题
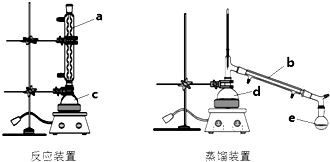
(1)写出合成乙酸乙酯的化学方程式CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.
(2)仪器b的名称冷凝管,图中起冷凝回流作用的是a(填a、b、c、d、e).
(3)为了提高乙酸乙酯的产率可采取的措施将CH3COOCH2CH3及时蒸馏分离;反应温度不宜过高,减少CH3COOHCH3CH2OH的挥发;反应物控制无水条件,浓硫酸的吸水作用有利于平衡向正反应方向移动,提高产率
(4)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
根据上表分析,蒸馏后得到的乙酸乙酯中,最有可能含有CH3CH2OH杂质.
0 158390 158398 158404 158408 158414 158416 158420 158426 158428 158434 158440 158444 158446 158450 158456 158458 158464 158468 158470 158474 158476 158480 158482 158484 158485 158486 158488 158489 158490 158492 158494 158498 158500 158504 158506 158510 158516 158518 158524 158528 158530 158534 158540 158546 158548 158554 158558 158560 158566 158570 158576 158584 203614

(1)写出合成乙酸乙酯的化学方程式CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.(2)仪器b的名称冷凝管,图中起冷凝回流作用的是a(填a、b、c、d、e).
(3)为了提高乙酸乙酯的产率可采取的措施将CH3COOCH2CH3及时蒸馏分离;反应温度不宜过高,减少CH3COOHCH3CH2OH的挥发;反应物控制无水条件,浓硫酸的吸水作用有利于平衡向正反应方向移动,提高产率
(4)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
| 物质 | 98.3%浓硫酸 | 乙酸乙酯 | 乙酸 | 乙醇 | 乙醚 | 水 |
| 沸点 | 338℃, | 77.1℃ | 118℃ | 78.5℃ | 34.6℃ | 100℃ |