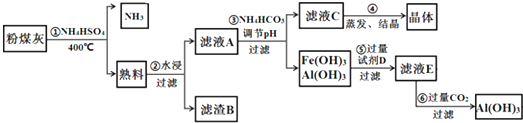
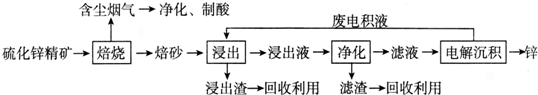
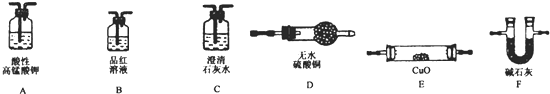
4.每年的6月26日是国际禁毒日,珍爱生命,远离毒品.以下是四种毒品的结构简式,下列有关说法正确的是( )


| A. | 冰毒的摩尔质量为149 | |
| B. | 海洛因和杜冷丁均能与溴水发生加成反应 | |
| C. | 1mol可卡因最多能与2molNaOH发生反应 | |
| D. | 以上毒品均属于芳香烃 |
3.已知某合金中除铝外,还含有铁、铜中的一种或两种,所含的金属都能通过化学方法检出.请设计合理的实验探究该合金中铁元素的存在.
仅限选择的用品:烧杯、试管、玻璃棒、量筒、容量瓶、胶头滴管、药匙、稀硫酸、稀硝酸、20%KSCN溶液、NaOH溶液.已知稀硝酸具有强氧化性,能将Fe氧化为Fe3+
完成以下实验探究过程:
(1)提出假设
猜想1:该合金中除铝外,还含有铁(填名称,下同).
猜想2:该合金中除铝外,还含有铜.
猜想3:该该合金中除铝外,还含有铁、铜.
(2)设计实验方案.基于猜想3设计出实验方案
(3)实验过程.根据(2)的实验方案,补充下表中的实验操作、预期现象和结论.
探究结论.猜想3成立(填″猜想1″″猜想2″或″猜想3″).
仅限选择的用品:烧杯、试管、玻璃棒、量筒、容量瓶、胶头滴管、药匙、稀硫酸、稀硝酸、20%KSCN溶液、NaOH溶液.已知稀硝酸具有强氧化性,能将Fe氧化为Fe3+
完成以下实验探究过程:
(1)提出假设
猜想1:该合金中除铝外,还含有铁(填名称,下同).
猜想2:该合金中除铝外,还含有铜.
猜想3:该该合金中除铝外,还含有铁、铜.
(2)设计实验方案.基于猜想3设计出实验方案
(3)实验过程.根据(2)的实验方案,补充下表中的实验操作、预期现象和结论.
| 步骤 | 实验方案 | 预期现象和结论 |
| ① | 用药匙取少许样品粉末,加入试管A中,再用胶头滴管取过量的NaOH溶液加入试管A中,充分反应后,静置.弃去上层清液,剩余固体备用. | 粉末部分溶解,并有气体放出,则合金中一定含有铝 |
| ② | 向试管A的剩余固体中加入过量的稀硫酸充分反应后,静置,取上层清液于试管B中,剩余固体备用. | 固体部分溶解,并有气体放出,溶液呈浅绿色,则合金中可能含有 铁. |
| ③ | 在试管B中加入少许稀硝酸,再滴加KSCN溶液 | 溶液先变成黄色,加KSCN后显血红色,结合②可知,一定含铁 |
| ④ | 往②剩余固体中加入稀硝酸,再滴加NaOH溶液 | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有蓝色沉淀产生,则合金中一定含有铜. |
2.元素X的原子核内只有1个质子.元素Y的阳离子电子层结构和氖原子电子层结构相同,Y、Z和E在周期表里位于同一周期.X和E、Z分别能形成气态氢化物XE和X2Z,它们的水溶液是酸.Z跟Y能形成离子化合物Y2Z.与氖同周期的元素F的气态氢化物FX3,其水溶液能使酚酞试液变红.则X、Y、Z、E、F的元素符号是( )
| A. | H、Na、S、Cl、N | B. | H、Na、S、Br、P | C. | H、Li、O、F、N | D. | H、Mg、S、O、N |
18.下列措施肯定能使化学反应速率增大的是( )
0 158384 158392 158398 158402 158408 158410 158414 158420 158422 158428 158434 158438 158440 158444 158450 158452 158458 158462 158464 158468 158470 158474 158476 158478 158479 158480 158482 158483 158484 158486 158488 158492 158494 158498 158500 158504 158510 158512 158518 158522 158524 158528 158534 158540 158542 158548 158552 158554 158560 158564 158570 158578 203614
| A. | 增加反应物的量 | B. | 增大反应体系的压强 | ||
| C. | 降低反应体系的温度 | D. | 使用适宜的催化剂 |
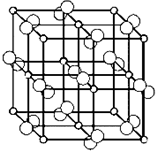 四川含有丰富的矿产资源,钒矿、钛矿、黄铁矿等七种矿产储量位居全国第1位.回答下列问题:
四川含有丰富的矿产资源,钒矿、钛矿、黄铁矿等七种矿产储量位居全国第1位.回答下列问题: 已知A、B、C、D、E都是周期表中前四周期原子序数依次增大的元素.其中A、B、C是同一周期的非金属元素.D与C可以形成两种常见的离子晶体,D的阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物M,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
已知A、B、C、D、E都是周期表中前四周期原子序数依次增大的元素.其中A、B、C是同一周期的非金属元素.D与C可以形成两种常见的离子晶体,D的阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物M,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)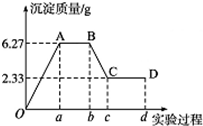 下面是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag +、Ca2+、Cl-、CO32-和SO42-中的若干种,该小组同学取100mL水样进行实验:向样品中先滴加硝酸钡溶液,再滴加1.0mol•L-1的硝酸,实验过程中沉淀质量的变化如图所示:
下面是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag +、Ca2+、Cl-、CO32-和SO42-中的若干种,该小组同学取100mL水样进行实验:向样品中先滴加硝酸钡溶液,再滴加1.0mol•L-1的硝酸,实验过程中沉淀质量的变化如图所示: