14.镧是重要的稀土元素,应用非常广泛,如应用于压电材料、催化剂等领域.

已知:
①镧是较活泼金属,在空气中易被氧化;
②氢氧化镧是难溶于水的弱碱;
③
(1)操作1、3是相同操作,其名称是过滤.
(2)操作2要在HCl气体的氛围内加热的原因是防止LaCl3水解.
(3)电解制镧的尾气要用碱液吸收,请写出反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(4)真空、高温过程中的反应方程式为3Ca+2LaF3$\frac{\underline{\;真空\;}}{高温}$3CaF2+2La.
(5)粗镧精制过程中温度控制范围1487~3470℃.
(6)重熔蒸馏制得的镧中仍然混有极少量的钙.某批次产品69.709g,经分析含钙0.209g,该产品的等级为分析纯(化工产品等级标准:优级纯≥99.8%,分析纯≥99.7%,化学纯≥99.5%)

已知:
①镧是较活泼金属,在空气中易被氧化;
②氢氧化镧是难溶于水的弱碱;
③
| 金 属 | 熔点(℃) | 沸点(℃) |
| 钙 | 841 | 1 487 |
| 镧 | 920 | 3 470 |
(2)操作2要在HCl气体的氛围内加热的原因是防止LaCl3水解.
(3)电解制镧的尾气要用碱液吸收,请写出反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(4)真空、高温过程中的反应方程式为3Ca+2LaF3$\frac{\underline{\;真空\;}}{高温}$3CaF2+2La.
(5)粗镧精制过程中温度控制范围1487~3470℃.
(6)重熔蒸馏制得的镧中仍然混有极少量的钙.某批次产品69.709g,经分析含钙0.209g,该产品的等级为分析纯(化工产品等级标准:优级纯≥99.8%,分析纯≥99.7%,化学纯≥99.5%)
12. 硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:
硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:
(1)测定蓝矾属于晶体的物理方法是X-射线衍射.其中SO42-中S原子的轨道杂化形式是sp3;H2O的空间构型是V形.
(2)将硫酸铜晶体加热到258~680℃生成的物质A,A是CuSO4(化学式);A溶于水配成溶液,加入氨水,观察到的现象是首先形成蓝色沉淀,继续加入氨水,沉淀溶解,得到深蓝色溶液;最终得到溶液中的含铜元素的离子是[Cu(NH3)4]2+(化学式),该离子含有的化学键类型有配位键、极性键.
(3)将硫酸铜晶体加热到1000℃以上生成的物质C,在C中的铜的离子的基态电子排布式是1s22s22p63s22p63d10;
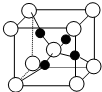
(4)如图是硫酸铜晶体分解得到一定温度的产物的晶胞(白球和黑球代表不同的原子).
①该温度是1000℃以上.
②铜原子的配位数是2.
③已知该晶体的密度为dg•cm-3,则晶胞参数是$\root{3}{\frac{288}{{N}_{A}d}}$×1010pm.
 硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:
硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:| 温度范围/℃ | 固体质量/g |
| 258~680 | 3.20 |
| 680~1000 | 1.60 |
| 1000以上 | 1.44 |
(2)将硫酸铜晶体加热到258~680℃生成的物质A,A是CuSO4(化学式);A溶于水配成溶液,加入氨水,观察到的现象是首先形成蓝色沉淀,继续加入氨水,沉淀溶解,得到深蓝色溶液;最终得到溶液中的含铜元素的离子是[Cu(NH3)4]2+(化学式),该离子含有的化学键类型有配位键、极性键.
(3)将硫酸铜晶体加热到1000℃以上生成的物质C,在C中的铜的离子的基态电子排布式是1s22s22p63s22p63d10;
(4)如图是硫酸铜晶体分解得到一定温度的产物的晶胞(白球和黑球代表不同的原子).
①该温度是1000℃以上.
②铜原子的配位数是2.
③已知该晶体的密度为dg•cm-3,则晶胞参数是$\root{3}{\frac{288}{{N}_{A}d}}$×1010pm.
9.利用铜萃取剂M,通过如下反应实现铜离子的富集(如图1):
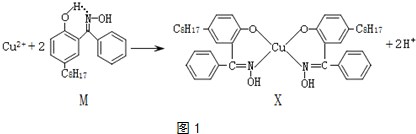
(1)X难溶于水、易溶于有机溶剂,其晶体类型为分子晶体.
(2)X中以sp2杂化、sp3杂化的原子的第一电离能由大到小顺序为N>O>C.
(3)上述反应中断裂和生成的化学键有be(填序号).
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(4)M与W(分子结构如图2)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
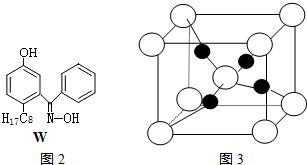
(5)硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒等功效.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如下表.回答下列问题:
图3是硫酸铜晶体分解得到一定温度的产物的晶胞(白球和黑球代表不同的原子).
①该温度是1000℃以上.
②铜原子的配位数是4.

(1)X难溶于水、易溶于有机溶剂,其晶体类型为分子晶体.
(2)X中以sp2杂化、sp3杂化的原子的第一电离能由大到小顺序为N>O>C.
(3)上述反应中断裂和生成的化学键有be(填序号).
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(4)M与W(分子结构如图2)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.

(5)硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒等功效.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如下表.回答下列问题:
| 温度范围/℃ | 固体质量/g |
| 258~680 | 3.20 |
| 680~1000 | 1.60 |
| 1000以上 | 1.44 |
①该温度是1000℃以上.
②铜原子的配位数是4.
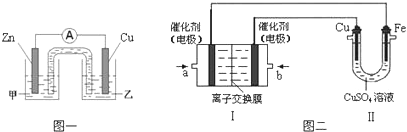
8. 对氨基苯酚(PAP)是一种重要的有机合成中间体,可用硝基苯(C6H5NO2)电解还原制备,装置如图所示.下列说法正确的是( )
对氨基苯酚(PAP)是一种重要的有机合成中间体,可用硝基苯(C6H5NO2)电解还原制备,装置如图所示.下列说法正确的是( )
 对氨基苯酚(PAP)是一种重要的有机合成中间体,可用硝基苯(C6H5NO2)电解还原制备,装置如图所示.下列说法正确的是( )
对氨基苯酚(PAP)是一种重要的有机合成中间体,可用硝基苯(C6H5NO2)电解还原制备,装置如图所示.下列说法正确的是( )| A. | 电解时Pt电极应与直流电源的负极相连 | |
| B. | 电解时Pt电极上有H2放出 | |
| C. | 阴极反应式为:C6H5NO2+4e-+4H+═HOC6H4NH2+H2O | |
| D. | 电解一段时间后,硫酸溶液的pH不变化 |
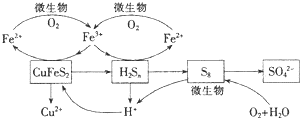
6.由黄铜矿(CuFeS2)制取铜的简单流程如图:

下列说法正确的是( )

下列说法正确的是( )
| A. | 由CuFeS2生成Cu2S,SO2和铁的氧化物反应中硫元素被还原 | |
| B. | 熔炼过程中的主要反应为:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2 | |
| C. | 铜的电解精炼过程中纯铜做阳极 | |
| D. | 上述冶炼过程产生大量SO2,通常用饱和NaHSO3溶液吸收 |
5.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示:
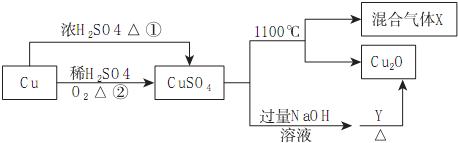
下列说法正确的是( )
0 158328 158336 158342 158346 158352 158354 158358 158364 158366 158372 158378 158382 158384 158388 158394 158396 158402 158406 158408 158412 158414 158418 158420 158422 158423 158424 158426 158427 158428 158430 158432 158436 158438 158442 158444 158448 158454 158456 158462 158466 158468 158472 158478 158484 158486 158492 158496 158498 158504 158508 158514 158522 203614

下列说法正确的是( )
| A. | 途径①和途径②都体现了硫酸的酸性和氧化性 | |
| B. | Y可以是乙醛溶液 | |
| C. | CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 | |
| D. | 将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体 |
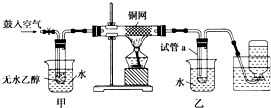 某实验小组用下列装置进行乙醇催化氧化的实验.
某实验小组用下列装置进行乙醇催化氧化的实验. 图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.
图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.