12.下列反应的离子方程式正确的是( )
| A. | Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O | |
| B. | 等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| C. | 向100mL 1mol/L FeBr2溶液中通入0.5mol Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| D. | 向澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O |
8.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素B的化合物可以用来做焰火材料 | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 元素B、D的最高价氧化物对应的水化物之间可能发生反应 |
7.下列离子方程式的书写正确的是( )
| A. | 漂白粉溶液中通入SO2气体 Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液 HCO3-+OH-═CO32-+H2O | |
| C. | 明矾溶液中加入过量的Ba(OH)2溶液2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| D. | 过量的NH4HSO4溶液与Ba(OH)2溶液反应2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
6.己知维生素A的结构简式可写为 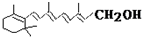 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )| A. | 维生素A的分子式为C20H32O | |
| B. | 维生素A不能使溴的四氯化碳溶液褪色 | |
| C. | 该有机物能发生取代反应 | |
| D. | 1mol维生素A 在催化剂作用下最多可与7molH2发生加成反应 |
5.有A、B、C、D、E五种短周期元素,其中A、B、C、D同周期,C、E同主族; A+与E2-具有相同的电子层结构;离子半径:C2->D-;B的单质晶体熔点、硬度大,是一种重要的半导体材料.下列说法中,正确的是( )
| A. | 由于D、C、E元素的氢化物相对分子质量依次减小,所以其沸点依次降低 | |
| B. | 元素D和E的某些单质不可以作为水处理中的消毒剂 | |
| C. | 元素B的单质只能与氢氧化钠溶液反应而不能与任何酸反应 | |
| D. | A、E两种元素能形成A2E和A2E2型化合物 |
4.设NA表示阿伏加德罗常数数值,下列叙述中正确的是( )
0 158298 158306 158312 158316 158322 158324 158328 158334 158336 158342 158348 158352 158354 158358 158364 158366 158372 158376 158378 158382 158384 158388 158390 158392 158393 158394 158396 158397 158398 158400 158402 158406 158408 158412 158414 158418 158424 158426 158432 158436 158438 158442 158448 158454 158456 158462 158466 158468 158474 158478 158484 158492 203614
| A. | 1.8 g的NH4+离子中含有的电子数为0.1NA | |
| B. | 1mol Na2O2 固体中含离子总数为4NA | |
| C. | 标准状况下,2.24L CCl4所含的共价键数为O.4NA | |
| D. | 常温常压下,92g NO2和N2O4的混合气体含有的原子数为6NA |

 .
. ,写出A生成B的反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,写出A生成B的反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.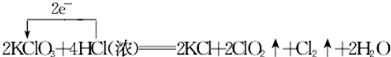 .
.