1.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解
(1)卤族元素位于周期表的p区
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在.使氢氟酸分子缔合的作用力是氢键
(3)请根据下表提供的第一电离能数据判断:理论上最有可能生成较稳定的单核阳离子的卤素原子是I(填名称或元素符号)
(4)已知高碘酸有两种形式,化学式分别为H5IO6(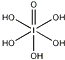 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
(5)已知ClO2-为V型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出与ClO3-互为等电子体的分子的分子式NCl3(写出1个)
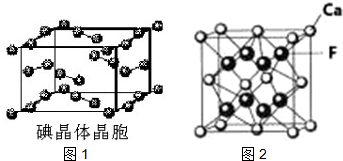
(6)如图1为碘晶体晶胞结构.有关说法中正确的是C
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以配位数4交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘分子间存在非极性键和范德华力
(7)已知CaF2晶体(图2)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻且最近的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$a3ρNA
(1)卤族元素位于周期表的p区
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在.使氢氟酸分子缔合的作用力是氢键
(3)请根据下表提供的第一电离能数据判断:理论上最有可能生成较稳定的单核阳离子的卤素原子是I(填名称或元素符号)
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)(5)已知ClO2-为V型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3,写出与ClO3-互为等电子体的分子的分子式NCl3(写出1个)
(6)如图1为碘晶体晶胞结构.有关说法中正确的是C
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以配位数4交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘分子间存在非极性键和范德华力
(7)已知CaF2晶体(图2)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻且最近的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{\sqrt{2}}{2}$a3ρNA

20.已知A是一种金属单质,B显淡黄色,其转化关系如图所示,则C的以下性质错误的是( )
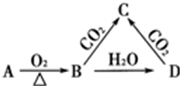

| A. | 与足量盐酸反应放出气体 | B. | 与澄清石灰水反应产生白色沉淀 | ||
| C. | 与氯化钙溶液不反应 | D. | 溶液呈碱性 |
18.下列关于有机化合物的认识不正确的是( )
| A. | 油脂在空气中完全燃烧转化为水和二氧化碳 | |
| B. | 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 | |
| C. | 在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应 | |
| D. | 在水溶液里,乙酸分子中的-CH3可以电离出H+ |
16.分子式为C4H8的各种同分异构体共有( )种.
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
15.下列物质中,属于芳香烃且属于苯的同系物的是( )
| A. |  | B. |  | C. |  | D. |  |
13.下列说法正确的是( )
0 158289 158297 158303 158307 158313 158315 158319 158325 158327 158333 158339 158343 158345 158349 158355 158357 158363 158367 158369 158373 158375 158379 158381 158383 158384 158385 158387 158388 158389 158391 158393 158397 158399 158403 158405 158409 158415 158417 158423 158427 158429 158433 158439 158445 158447 158453 158457 158459 158465 158469 158475 158483 203614
| A. | HF、HCl、HBr、HI的溶沸点依次升高 | |
| B. | 在气态单质分子中,一定存在共价键 | |
| C. | 只含离子键的化合物才是离子化合物 | |
| D. | 在共价化合物中,一定存在着共价键 |
 .一定条件下,硫与地壳中含量最多的非金属元素X可组成两种常见的化合物,则X是O,两种化合物均含有的化学键为共价键
.一定条件下,硫与地壳中含量最多的非金属元素X可组成两种常见的化合物,则X是O,两种化合物均含有的化学键为共价键
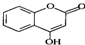 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成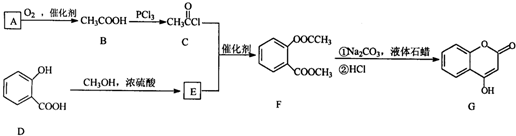
 .
.

 .
. .
.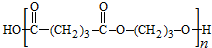 .
.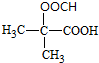 (写结构简式).
(写结构简式).