1.“泰诺林”是治疗感冒发烧的一种药物.其主要成份的结构简式如下: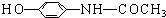 下列关于该物质的描述,不正确的是( )
下列关于该物质的描述,不正确的是( )
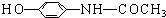 下列关于该物质的描述,不正确的是( )
下列关于该物质的描述,不正确的是( )| A. | 该化合物分子式为C8H9O2N | |
| B. | 能和银氨溶液发生银镜反应 | |
| C. | 能和氢氧化钠发生反应 | |
| D. | 其分子中的原子不可能都在同一平面上 |
20.短周期元素R的原子最外层电子数比次外层电子数少2个.下列说法正确的是( )
| A. | R有多种氧化物 | B. | R的气态氢化物很稳定 | ||
| C. | R的非金属性比Cl的非金属性强 | D. | R的最高价氧化物的水化物是强碱 |
19.下列粒子的核外电子排布正确的是( )
| A. | Na  | B. | K  | C. | Xe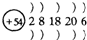 | D. | Cl- |
15.锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]3d104s24p2,有2个未成对电子.
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键.从原子结构角度分析,原因是Ge原子半径大,原子间形成的σ单键较长,p-p轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键.
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因GeCl4、GeBr4、GeI4的熔、沸点依次增高.原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强.
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂.Zn、Ge、O电负性由大至小的顺序是O>Ge>Zn.
(5)①Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为sp3,微粒之间存在的作用力是共价键.
②已知Ge单晶的晶胞的边长为565.76pm,其密度为$\frac{8×73}{6.02×1{0}^{23}×(565.76×1{0}^{-10})^{3}}$g•cm-3(列出计算式即可,阿伏加德罗常数用NA表示,Ge的相对原子质量为73).
(1)基态Ge原子的核外电子排布式为[Ar]3d104s24p2,有2个未成对电子.
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键.从原子结构角度分析,原因是Ge原子半径大,原子间形成的σ单键较长,p-p轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键.
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因GeCl4、GeBr4、GeI4的熔、沸点依次增高.原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强.
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(5)①Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为sp3,微粒之间存在的作用力是共价键.
②已知Ge单晶的晶胞的边长为565.76pm,其密度为$\frac{8×73}{6.02×1{0}^{23}×(565.76×1{0}^{-10})^{3}}$g•cm-3(列出计算式即可,阿伏加德罗常数用NA表示,Ge的相对原子质量为73).
14.今年我国中南部遭受了50年一遇的大旱,在抽取地下水为饮用水的处理中,不恰当的是( )
| A. | 杀菌消毒 | B. | 静置沉淀 | C. | 煮沸 | D. | 直接饮用 |
13.下列能源既清洁又可再生的是( )
0 158285 158293 158299 158303 158309 158311 158315 158321 158323 158329 158335 158339 158341 158345 158351 158353 158359 158363 158365 158369 158371 158375 158377 158379 158380 158381 158383 158384 158385 158387 158389 158393 158395 158399 158401 158405 158411 158413 158419 158423 158425 158429 158435 158441 158443 158449 158453 158455 158461 158465 158471 158479 203614
| A. | 煤 | B. | 天然气 | C. | 汽油 | D. | 氢气 |
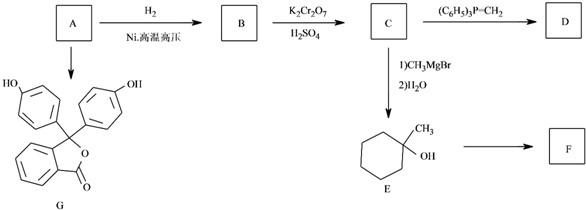
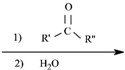
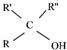
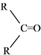 $\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$
$\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$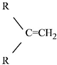 (R表示烃基,R′和R″表示烃基或基)
(R表示烃基,R′和R″表示烃基或基) .
. 、
、 .
. .
. .
. .
.